
| 序号 | 实验操作 | 实验目的 |
| A | 在浓硫酸和稀硫酸中分别加入Cu片,加热 | 比较稀、浓硫酸氧化性强弱 |
| B | F2、Cl2分别与H2反应 | 比较氟、氯的非金属性强弱 |
| C | 把CO2通入到水玻璃中 | 比较碳、硅的非金属性强弱 |
| D | 向MgCl2、AlCl3溶液中分别通入NH3 | 比较镁、铝金属性强弱 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.浓硫酸加热条件下能与铜反应;
B.非金属性越强,单质与氢气化合越容易;
C.最高价氧化物的水化物的酸性越强,该元素的非金属性越强;
D.MgCl2、AlCl3溶液与氨气反应的现象相同.
解答 解:A.浓硫酸加热条件下能与铜反应,稀硫酸不反应,可证明,故A正确;
B.非金属性越强,单质与氢气化合越容易,所以可以根据F2、Cl2分别与H2反应来判断F、Br的非金属性强弱,故B正确;
C.强酸反应制弱酸,碳酸的酸性大于硅酸,从而说明碳的非金属性比硅的强,故C正确;
D.MgCl2、AlCl3溶液与氨气反应的现象相同,所以不能根据MgCl2、AlCl3溶液与氨气来比较Mg、Al的非金属性强弱,故D错误.
故选D.
点评 本题考查了金属性和非金属性强弱的判断方法,题目难度不大,侧重于从实验的角度来考查,注意基础知识的积累.


科目:高中化学 来源: 题型:解答题
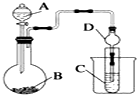 某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验.
某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
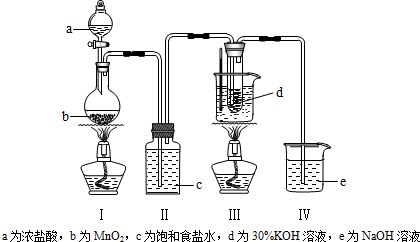
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
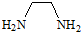 )在一定条件下发生反应生成1mol EDTA和4mol HCl,则EDTA的分子式为( )
)在一定条件下发生反应生成1mol EDTA和4mol HCl,则EDTA的分子式为( )| A. | C10H16N2O8 | B. | C10H20N2O8 | C. | C8H16N2O8 | D. | C16H20N2O8Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
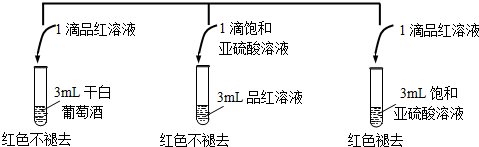
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将水蒸气通过灼热的铁粉 | 粉末变红 | 铁与水在高温下反应 |
| B | 将可调高度的铜丝伸入到HNO3中 | 溶液变蓝 | Cu与稀HNO3发生置换反应 |
| C | 将浓硫酸滴到蔗糖表面 | 固体变黑 | 浓硫酸具有脱水性和强酸性 |
| D | 将KI和FeCl3溶液在试管中混合后,加入CCl4,振荡,静置 | 下层溶液显紫红色 | 氧化性:Fe3+>I2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com