
| 组号 | 反应温度/℃ | Na2S2O3 | H2SO4 | H2O体积/mL | ||
| 体积/mL | 浓度/mol?L-1 | 体积/mL | 浓度/mol?L-1 | |||
| A | 10 | 5 | 0.2 | 5 | 0.1 | 10 |
| B | 10 | 5 | 0.1 | 5 | 0.1 | 10 |
| C | 30 | 5 | 0.1 | 5 | 0.1 | 10 |
| D | 30 | 5 | 0.2 | 5 | 0.2 | 10 |
| A、A | B、B | C、C | D、D |
 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:
| A、稀硫酸跟铁反应:Fe+6H+=2Fe3++3H2↑ |
| B、稀硫酸与氢氧化钡溶液反应:H++OH-=H2O |
| C、碳酸钙放入稀盐酸中:CO32+2H+=CO2↑+H2O |
| D、稀盐酸放入碳酸钠中:CO32+2H+=CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
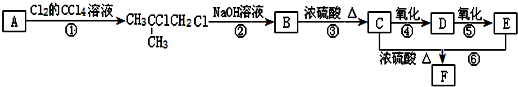
查看答案和解析>>
科目:高中化学 来源: 题型:
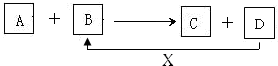
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、12 | B、22 | C、24 | D、30 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、气体使湿润的酚酞试液变红 |
| B、气体能使湿润的红色石蕊试纸变蓝 |
| C、气体与蘸有浓H2SO4的玻璃棒靠近 |
| D、气体与蘸有浓盐酸的玻璃棒靠近 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 用二氧化氯、铁酸钠(Na2FeO4)等新型净水剂替代传统的净水剂Cl2对淡水进行消毒是城市饮用水处理新技术,ClO2和Na2FeO4在水处理过程中分别被还原为Cl-和Fe3+.
用二氧化氯、铁酸钠(Na2FeO4)等新型净水剂替代传统的净水剂Cl2对淡水进行消毒是城市饮用水处理新技术,ClO2和Na2FeO4在水处理过程中分别被还原为Cl-和Fe3+.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com