


科目:高中化学 来源: 题型:
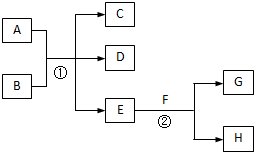 在下列各变化中,E为无色无味的液体(常温下),F为淡黄色粉末,G为常见的无色气体(反应条件均已省略).
在下列各变化中,E为无色无味的液体(常温下),F为淡黄色粉末,G为常见的无色气体(反应条件均已省略).查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、氧化剂是MnO2,还原剂是HCl |
| B、每生成1mol Cl2,转移电子的物质的量为2mol |
| C、每消耗1mol MnO2,起还原剂作用的HCl消耗4mol |
| D、转移电子的物质的量为1mol时,生成标准状况下Cl2的体积为11.2L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙醇(水):加入新制生石灰,蒸馏 |
| B、乙酸乙酯(乙醇):加入NaOH溶液,振荡静置后分液 |
| C、乙酸(乙醇):加入金属钠,蒸馏 |
| D、溴苯(溴):加入NaOH溶液,充分振荡静置后,分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下浓硫酸与铝不发生反应,可在常温下用铝制容器贮藏贮运浓硫酸 |
| B、二氧化硅不与任何酸反应,可用石英制造耐酸容器 |
| C、二氧化氯具有氧化性,可用于自来水的杀菌消毒 |
| D、铜的金属活泼性比铁的弱,可在海轮外壳上装若干铜块以减缓其腐蚀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com