
 我校环保兴趣小组在处理污水样品时,需用质量分数为36.5%的浓盐酸、密度为1.19g/cm3)配制成250mL 0.1mol•L-1的盐酸溶液.
我校环保兴趣小组在处理污水样品时,需用质量分数为36.5%的浓盐酸、密度为1.19g/cm3)配制成250mL 0.1mol•L-1的盐酸溶液.分析 (1)根据配制一定物质的量浓度的溶液使用的仪器分析需要的仪器和缺少的仪器;再根据玻璃棒在操作中的作用解答;
(2)根据c=$\frac{1000ωρ}{M}$计算出需要浓盐酸的浓度,再根据溶液稀释过程中溶质的物质的量不变计算需要的氯化氢的体积,据此选择量筒规格;
(3)配制一定物质的量浓度的溶液操作步骤解答;
(4)根据容量瓶的构造及正确使用方法进行判断;
(5)根据c=$\frac{n}{V}$,误差分析时,关键要看配制过程中引起n和V怎样的变化,若n比理论值小或V比理论值大时,都会使所配溶液浓度偏小;若n比理论值大或V比理论值小时,都会使所配溶液浓度偏大.
解答 解:(1)配制一定物质的量浓度的溶液使用的仪器:量筒、烧杯、玻璃棒、容量瓶、胶头滴管,用不大分液漏斗;还缺少玻璃棒;玻璃棒在稀释时起到搅拌作用;在移液时起到引流作用;
故答案为:C;玻璃棒;搅拌;引流;
(2)质量分数为36.5%的浓盐酸、密度为1.19g/cm3)的物质的量浓度C=$\frac{1000×1.19×36.5%}{36.5}$=11.9mol/L,设需要浓盐酸体积为V,则根据溶液稀释过程中溶质的物质的量不变计算得:V×11.9mol/L=250mL×0.1mol•L-1,解得:V=2.1mL,所以应选择10mL量筒;
故选:A;
(3)配制一定物质的量浓度的溶液操作步骤:计算、量取、稀释、冷却、移液、洗涤、定容、摇匀,所以正确的顺序为:③①④②;
故答案为:③①④②;
(4)A、容量瓶使用时,应先检查是否漏水,然后用蒸馏水洗涤干净即可,故A正确;
B、容量瓶洗净后不能用所配制溶液润洗,否则影响配制的溶液的浓度,故B错误;
C、容量瓶只能用来配制溶液,不能在容量瓶中溶解,应该在烧杯中溶解,故C错误;
D、容量瓶只能用来配制溶液,不能在容量瓶中稀释,应该在烧杯中稀释,故D错误;
E、摇匀时,盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转,故E正确;
故选AE;
(5)①容量瓶中有少量蒸馏水,对溶质的物质的量和溶液体积都不会产生影响,溶液浓度不变,故选c;
②烧杯和玻棒没有洗涤2-3次,导致部分溶质损失,溶质的物质的量偏小,溶液浓度偏低,故选b;
③稀释浓HCl时,没有冷却就立即转移到容量瓶中,冷却后溶液体积偏小,溶液浓度偏高,故选a;
④配制的溶液装入洁净的但有少量蒸馏水的试剂瓶中,导致将配制溶液稀释,溶液浓度偏低,故选b;
⑤若定容时俯视,所配溶液的物质的量浓度,导致溶液的体积偏小,溶液浓偏高,故选a;
故答案为:c;b;a;b;a.
点评 本题考查了一定物质的量浓度溶液的配制,明确配制原理和操作过程即可解答,注意容量瓶、量筒规格的选择,注意误差分析的方法.


科目:高中化学 来源: 题型:解答题

| 物质 | 溶点/℃ | 沸点/℃ | 其他 |
| CCl4 | -23 | 76 | 与TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮湿空气产生白雾 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 探究温度对反应速率影响时,分别水浴加热硫代硫酸钠溶液、硫酸溶液到一定温度,再将两溶液混合 | |
| B. | H2O2在过氧化氢酶的催化下,随着温度的升高,分解速率持续加快 | |
| C. | 用简易量热计测定反应热,使用碎泡沫隔热保温、环形玻璃搅拌棒搅拌、量取达到的最高温度,计算反应热,取2~3 次的实验平均值 | |
| D. | 取皂化反应后的混合液滴入热水中,观察现象,可判断皂化反应是否完全 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{b-2c}{a}$mol.L-1 | B. | $\frac{2b-c}{a}$mol.L-1 | C. | $\frac{a-b}{a}$mol.L-1 | D. | $\frac{2b-4c}{a}$mol.L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含ⅥA族元素的化合物在研究和生产中有许多重要用途.请回答下列问题:
ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含ⅥA族元素的化合物在研究和生产中有许多重要用途.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol的甲基(-CH3)与羟基(-OH)所含电子数均为NA | |
| B. | 1molD216O中含中子、质子、电子各10NA | |
| C. | 32 g S8单质(分子结构如右图)中含有的S-S键个数为NA | |
| D. | 1.5g CH3+中含有的电子数为0.8NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 容 器 | 甲 | 乙 |
| 反应物投入量 | 3mol H2、2mol N2 | 6mol H2、4mol N2 |
| 达到平衡的时间(min) | t | 5 |
| 平衡时N2的浓度(mol•L-1) | 3 | c |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  实验室中制取少量的乙酸乙酯 | |
| B. |  比较硫、碳、硅三种元素的非金属性强弱 | |
| C. |  处理尾气 | |
| D. | 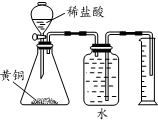 测定黄铜(Cu、Zn合金)中Zn 的含量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com