
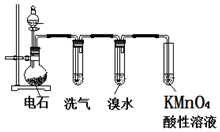
 如图为实验室制取乙炔并验证其性质的装置图,回答下列问题:
如图为实验室制取乙炔并验证其性质的装置图,回答下列问题: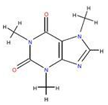 ,实验室可通过下列简单方法从茶叶中提取咖啡因:
,实验室可通过下列简单方法从茶叶中提取咖啡因: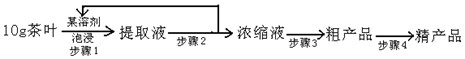
分析 实验室用电石和水反应制备乙炔,其中含有杂质,为了净化和检验乙炔气体,测定气体体积,则需要的装备依次为:气体制备装置、净化装置(除硫化氢)、检验装置、性质实验装置、排水测体积的装置,
(1)制备乙炔碳化钙与水反应很剧烈,用饱和食盐水可以减缓反应;
(2)实验室制备乙炔是利用电石和水反应生成乙炔和氢氧化钙;
(3)电石中含有硫化钙杂质,所以制备的乙炔气体中往往含有少量的H2S气体,会干扰后续检验实验;
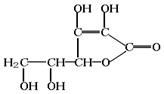
咖啡因易溶于氯仿、乙醇、丙酮及热苯等,微溶于水、石油醚,则步骤1可加入乙醇等有机溶剂进行萃取,然后进行蒸馏、升华,可得到咖啡因粗产品,
(4)咖啡因易溶于氯仿、乙醇、丙酮及热苯等,微溶于水、石油醚等,可进行萃取;
(5)分离咖啡因和乙醇,可进行加热得到浓缩液再结晶(或蒸发)得到粗产品,因咖啡因易升华,为进一步得到较为纯净的咖啡因,可进行升华.
解答 解:(1)实验室制备乙炔碳化钙与水反应很剧烈,用饱和食盐水可以减缓反应,所以为了得到平稳的气流,用饱和食盐水代替水,则分液漏斗中盛放的液体是饱和食盐水,故答案为:饱和食盐水;
(2)实验室制备乙炔是利用电石和水反应生成乙炔和氢氧化钙,反应的化学方程式为:CaC2+2H2O→CH≡CH↑+Ca(OH)2,
故答案为:CaC2+2H2O→CH≡CH↑+Ca(OH)2;
(3)电石中含有硫化钙杂质,所以制备的乙炔气体中往往含有少量的H2S气体,硫化氢气体具有还原性,也会导致溴水、高锰酸钾溶液褪色,所以洗气中应选CuSO4溶液或NaOH溶液除去乙炔中的硫化氢;故答案为:CuSO4溶液或NaOH溶液;
(4)咖啡因易溶于氯仿、乙醇、丙酮及热苯等,微溶于水、石油醚,则步骤1可加入乙醇等有机溶剂进行萃取,故答案为:B;
(5)分离咖啡因和乙醇,可进行加热得到浓缩液再结晶(或蒸发)得到粗产品,因咖啡因易升华,为进一步得到较为纯净的咖啡因,可进行升华,故答案为:结晶(或蒸发).
点评 本题考查乙炔制备、检验和物质的分离、提纯,为高考常见题型,侧重于学生的分析、实验能力的考查,注意把握题给信息以及实验流程,掌握实验基本操作和实验设计方法是解题关键,难度不大.


科目:高中化学 来源: 题型:解答题
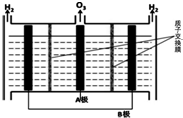 NO能引起光化学烟雾,破坏臭氧层.处理NO有多种方法,根据题意回答下列问题:
NO能引起光化学烟雾,破坏臭氧层.处理NO有多种方法,根据题意回答下列问题:| 时间(s) | 0 | 1 | 2 | 3 | 4 | … |
| c(NO)/mol•L-1 | 1.00×10-3 | 4.00×10-4 | 1.70×10-4 | 1.00×10-4 | 1.00×10-4 | … |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子数:N2<O2 | B. | 气体摩尔体积:N2<O2 | ||
| C. | 气体的压强:N2<O2 | D. | 体积:N2<O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,其中氮的化合价为-2.
,其中氮的化合价为-2.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
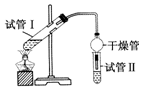 乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业.实验室制备乙酸乙酯的化学方程式如下:CH3COOH+C2H5OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOC2H5+H2O
乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业.实验室制备乙酸乙酯的化学方程式如下:CH3COOH+C2H5OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOC2H5+H2O| 实验编号 | 试管Ⅰ中试剂 | 试管Ⅱ中试剂 | 测得有机层的厚度/cm |
| A | 3mL乙醇、2mL乙酸、1mL 18mol•L-1浓H2SO4 | 饱和Na2CO3溶液 | 5.0 |
| B | 3mL乙醇、2mL乙酸 | 0.1 | |
| C | 3mL乙醇、2mL乙酸、6mL 3mol•L-1 H2SO4 | 1.2 | |
| D | 3mL乙醇、2mL乙酸、盐酸 | 1.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当X是盐酸时,则F是稀硝酸24 | |
| B. | 当X是氢氧化钠时,则F是稀硝酸y | |
| C. | 当X是氢氧化钠时,B跟Cl2反应可能有白烟现象e | |
| D. | 当X是氢氧化钠时,B能使酸性高锰酸钾溶液褪色N |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
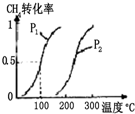 甲醇被称为21世纪的新型燃料,工业上用CH4和H2O为原料通过下列反应①和②,
甲醇被称为21世纪的新型燃料,工业上用CH4和H2O为原料通过下列反应①和②,| 实验编号 | T(°C) | n(CO)/n(H2) | p(MPa) |
| Ⅰ | 150 | 1/3 | 0.1 |
| Ⅱ | 5 | ||
| Ⅲ | 350 | 5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com