
����Ŀ��2009��12��7�ա�18���ڵ������籾�����ٿ������������ᣬ���֡������鶨�顷һ�ڳ�ŵ���ں�ĺ�����������2012����2020���ȫ�����Э�飬��ᳫ�������ܼ��š��͡���̼���á������ʹ�����CO2�ĺ�������Ч�ؿ�������CO2 �� �����˸������ձ����ӣ������ŷ�CO2����ɡ�����ЧӦ������ѧ�������о���ν�CO2ת��Ϊ�����õ���Դ��Ŀǰ��ҵ����һ�ַ�������CO2������ȼ�ϼ״���һ�������·�����Ӧ��CO2��g��+3H2��g��CH3OH��g��+H2O��g����ͼ1��ʾ�÷�Ӧ��������������λΪkJmol��1���ı仯��

��1�����ڸ÷�Ӧ������˵���У���ȷ����������ĸ����
A.��H��0����S��0
B.��H��0����S��0
C.��H��0����S��0
D.��H��0����S��0
��2��Ϊ̽����Ӧԭ�����ֽ�������ʵ�飬�����Ϊl L���ܱ������У�����l mol CO2��3mol H2 �� һ�������·�����Ӧ��CO2��g��+3H2��g��CH3OH��g��+H2O��g���������CO2��CH3OH��g����Ũ����ʱ��仯��ͼ2��ʾ��
�ٴӷ�Ӧ��ʼ��ƽ�⣬CO2��ƽ����Ӧ����v��CO2��= ��
�ڸ÷�Ӧ��ƽ�ⳣ������ʽK= ��
�����д�ʩ����ʹ��ѧƽ��������Ӧ�����ƶ�����������ĸ����
A�������¶� B����CH3OH��g����ʱҺ�����
C��ѡ���Ч���� D���ٳ���l molCO2��3molH2
��3��25�棬1.01��105Paʱ��16g Һ̬�״���ȫȼ�գ����ָ���ԭ״̬ʱ���ų�369.2kJ��������д���÷�Ӧ���Ȼ�ѧ����ʽ�� ��
���𰸡�
��1��C
��2��0.075mol/��L?min����![]() ��BD
��BD
��3��CH3OH��l�� +![]() O2��g��=CO2��g��+2H2O��l����H=��738.4kJ?mol��1
O2��g��=CO2��g��+2H2O��l����H=��738.4kJ?mol��1
����������1�����ݷ�Ӧ��ͼ������жϣ�CO2��g��+3H2��g��CH3OH��g��+H2O��g������Ӧ���ؼ��ٵķ�Ӧ��S��0����Ӧ������������������������жϷ�Ӧ�Ƿ��ȷ�Ӧ����H��0��
��2��������̼�Ƿ�Ӧ���淴Ӧ����Ũ�ȼ�С���״���������淴Ӧ����Ũ������10nim�ڴﵽƽ�⣬���ɼ״�Ũ��Ϊ0.75mol/L��������̼Ũ�ȱ仯��0.75mol/L��������ݻ�ѧƽ����ʽ����Ϊ��
CO2��g��+3H2��g��CH3OH��g��+H2O��g��
��ʼ����mol/L�� 1 3 0 0
�仯����mol/L�� 0.75 2.25 0.75 0.75
ƽ������mol/L�� 0.25 0.75 0.75 0.75
CO2��ƽ����Ӧ����v��CO2��= ![]() =0.075molL��1min��1 �� ���Դ��ǣ�0.075 molL��1min��1��
=0.075molL��1min��1 �� ���Դ��ǣ�0.075 molL��1min��1��
�ڸ÷�Ӧ��ƽ�ⳣ������ʽK= ![]()
�۴�ʩ����ʹ��ѧƽ��������Ӧ�����ƶ����ǣ�A����Ӧ�Ƿ��ȷ�Ӧ������ƽ��������У���A����B����CH3OH��g����ʱҺ���������С�����������ƽ��������У���B��ȷ��
C��ѡ���Ч����ֻ�ܸı����ʣ����ı仯ѧƽ�⣬��C����D���ٳ���l molCO2��4molH2 �� ����ѹǿƽ��������У���D��ȷ����ѡBD����3��25�棬1.01��105Paʱ��16g Һ̬�״����ʵ���Ϊ0.5mol����ȫȼ�գ����ָ���ԭ״̬ʱ���ų�369.2kJ��������������д�Ȼ�ѧ����ʽ�ķ���д���÷�Ӧ���Ȼ�ѧ����ʽΪ��CH3OH��l��+ ![]() O2��g��=CO2��g��+2H2O��l����H=��738.4 kJmol��1��
O2��g��=CO2��g��+2H2O��l����H=��738.4 kJmol��1��
�����㾫����ͨ��������û�ѧƽ��״̬���ʼ����������ջ�ѧƽ��״̬�����������ȡ��� V��=V��>0�����������Ƕ�̬ƽ�⣬ƽ��ʱ��Ӧ���ڽ��У�����������Ӧ������и���ְٷֺ������䣻���䡱�������ı䣬ƽ�ⱻ���ƣ������µ������½����µĻ�ѧƽ�⣻��;���أ�����������䣬���淴Ӧ�����Ǵ�����Ӧ��ʼ�����Ǵ��淴Ӧ��ʼ�����ɽ���ͬһƽ��״̬����Ч�������Խ����⣮


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ȷ����( )
A. ����Һ����Һ�������������
B. �������Ӧʱ��ϡ������ܱ���ԭΪ���ͼ�̬��ϡ����������ǿ��Ũ����
C. ��������ֽ⣬��������̬����ʱҪ�ܷⱣ�棬����������ͨ�紦
D. ϡ����ͻ��ý�����Ӧʱ�ò�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����( )
A. ú�ĸ�����Ǽ��ȳ�ȥú�е�ˮ�֣��õ������̿
B. ú�к��мױ������ױ��ȣ���ͨ������õ�
C. ��úΪ��Ҫԭ�ϣ����Ժϳɼ״�
D. ú����õ��Ľ�¯����������ˮ��Ӧ��ʹ��ˮ��ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ʺ�����ԭ����Ŀ�����ǣ� ��
A. 0.3mol HNO3 B. 0.3mol H2O
C. 0.1molH3PO4 D. 0.2molCH4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֬����������ȫˮ��IJ����Ǹ�֬����ͣ� ��
A.������
B.����
C.��̪
D.������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������������Ҫ��Ӧ�ǣ�4NH3��g��+5O2��g��4NO��g��+6H2O��g��
��1���ٸ÷�Ӧ���ر��S0�����������������=������
�������¶ȣ���Ӧ��ƽ�ⳣ��Kֵ��С����÷�Ӧ���ʱ��H0�����������������=������
��2���������������䣬���й�ϵͼ���������ѡ����ţ���
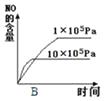


��3�����ݻ��̶����ܱ������з���������Ӧ�������ڸ����ʵ�Ũ�����±���
ʱ��/Ũ��/��molL��1�� | c��NH3�� | c��O2�� | c��NO�� | c��H2O�� |
��ʼ | 4.0 | 5.5 | 0 | 0 |
�� 2min | 3.2 | 4.5 | 0.8 | 1.2 |
�� 4min | 2.0 | 3.0 | 2.0 | 3.0 |
�� 6min | 2.0 | 3.0 | 2.0 | 3.0 |
�ٷ�Ӧ�ڵ�2min����4minʱ����Ӧ���ʦԣ�O2��=��
�ڷ�Ӧ�ڵ�2minʱ�ı����������ı������������ �� �������£���Ӧ��ƽ�ⳣ��K=��ֻд�����������굥λ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ���ʵ����̽��Ԫ�����ʵĵݱ���ɣ�ʵ��װ����ͼ��ʾ��
ʵ�����Ԫ����ۺ����������ǿ��̽��Ԫ�طǽ����Եݱ���ɡ�
��֪Aװ�õ���ƿ��װ�д���ʯ����Һ©����װ��ϡHNO3 �� Bװ����װ�б���̼��������Һ��Cװ����װ��Na2SiO3��Һ���Իش�
��1��A�з�Ӧ�����ӷ���ʽΪ �� C�пɹ۲쵽����������
��2��Bװ�õ���������
��3������ʵ��������֪��̼�ᡢ���ᡢ���������ǿ��˳���� �� �ɴ˵ó�̼���衢������Ԫ�طǽ����Ե�ǿ��˳������
��4��ʵ�����֪�����¸��������Ũ�����Ͽɲ������������ø�װ��̽���Ⱥ���Ԫ�صķǽ�����ǿ����
д��Bװ���з�����Ӧ�����ӷ���ʽ����
��5��Cװ�õ���������
��6��ʵ����ۣ������� �� �ǽ����ԣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ��(����)
A. ��������ԭ��Ӧ������������������
B. ��������ԭ��Ӧ��������������
C. ���ֽⷴӦҲ������������ԭ��Ӧ
D. û�е��ʲμӵĻ��Ϸ�Ӧһ������������ԭ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D������ѧ��ѧ�г������ʣ�����A��B��C������ͬһ��Ԫ�أ���һ���������ת����ϵ���ң����ַ�Ӧ�е�ˮ����ȥ���� 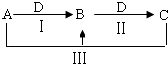
��1����AΪ�ȼҵ�IJ�Ʒ��CΪ�����е���Ʒ��
��D�ĵ���ʽ�� ��
�ڷ�Ӧ������ӷ���ʽ�� ��
���ȼҵ�Ʊ�A�Ļ�ѧ����ʽ�� �� �������ֲ������KI��Һ��Ӧ�Ƶ�һ�ֻ���ԭ�ϣ�������0.1mol KIת�Ƶ���0.6mol�����������ʼ䷴Ӧ�����ӷ���ʽ�� ��
��2����A��D��Ϊ���ʣ���AΪ���壬DԪ�ص�һ�ֺ���ɫ�����ﳣ�������ϣ�
�ٷ�Ӧ������ӷ���ʽ�� ��
��B������ˮ������ʹ��ʱ����B����ʹ���Է�ˮ�е������������ȥ����ԭ���� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com