
下列实验操作导致所读出的数值比真实值小的是(假设其他操作均正确)
A.对滴定管仰视读数: 23. 80 mL
B.将胆矾置于托盘天平右盘称量所得质量10. 4 g(左盘祛码10 g,游码0.4 g)
C.中和热测定时用铜棒代替环形玻璃搅拌棒搅拌,测定反应的最高温度: 30. 4OC
D.用量筒量取硝酸时,俯视读数: 5. 8 mL
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:
短周期元素A、B、C、D、E原子序数依次增大。A是周期表中原子半径最小的元素,B是形成化合物种类最多的元素,C是自然界含量最多的元素,D是同周期中金属性最强的元素,E的负一价离子与C的某种氢化物W分子含有相同的电子数。
(1)A、C、D形成的化合物中含有的化学键类型为 ;W的电子式 。
(2)已知:①2E· → E-E;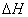 =-a kJ·mol-1 ② 2A· → A-A;
=-a kJ·mol-1 ② 2A· → A-A;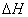 =-b kJ·mol-1 ③E·+A· → A-E;
=-b kJ·mol-1 ③E·+A· → A-E;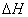 =-c kJ·mol-1
=-c kJ·mol-1
写出298K时,A2与E2反应的热化学方程式 。
(3)在某温度下、容积均为2L的三个密闭容器中,按不同方式投入反应物,保持恒温恒容,使之发生反应:2A2(g)+BC(g) X(g);
X(g);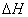 =-a KJ·mol-1(a>0,X为A、B、C三种元素组成的一种化合物)。初始投料与各容器达到平衡时的有关数据如下:
=-a KJ·mol-1(a>0,X为A、B、C三种元素组成的一种化合物)。初始投料与各容器达到平衡时的有关数据如下:
| 实验 | 甲 | 乙 | 丙 |
| 初始投料 | 2 mol A2、1 mol BC | 1 mol X | 4 mol A2、2 mol BC |
| 平衡时n(X) | 0.5mol | n2 | n3 |
| 反应的能量变化 | 放出Q1kJ | 吸收Q2kJ | 放出Q3kJ |
| 体系的压强 | P1 | P2 | P3 |
| 反应物的转化率 |
|
|
|
①在该温度下,假设甲容器从反应开始到平衡所需时间为4 min,则A2的平均反应速率 ( A2)为 。
( A2)为 。
②该温度下此反应的平衡常数K的值为 。
③下列现象能说明甲容器中的反应已经达到平衡状态的有 (填序号)。
A. 容器内A2、BC、X的物质的量之比为2:1:1
B. 容器内气体的密度保持恒定
C. 容器内A2气体的体积分数保持恒定
D.2V正(A2)=V逆(BC)
④三个容器中的反应分别达平衡时各组数据关系正确的是 (填序号)。
A.α1+α2=1 B.Q1+Q2=a C.α3<α1
D.P3<2P1=2P2 E.n2<n3<1.0mol F.Q3=2Q1
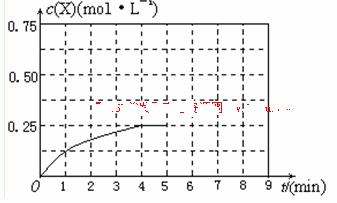
(4)在其他条件不变的情况下,将甲容器的体系体积压缩到1L,若在第8min达到新的平衡时A2的总转化率为75%,请在上图中画出第5min 到新平衡时X的物质的量浓度的变化曲线。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对化学实验现象的解释或结论正确的是
| 选项 | 事实 | 解释或结论 |
| A | 常温下,向饱和Na2CO3溶液中加入少量BaSO4粉末,过滤,向洗净的沉淀中加稀盐酸,产生气泡 | 常温下: Ksp(BaCO3)>Ksp(BaSO4) |
| B | 盐酸与亚硫酸钠反应,生成使品红试液褪色的气体 | 非金属性:Cl> S |
| C | 滴有酚酞的NaHCO3溶液呈浅红色,微热后红色加深 | NaHCO3分解生成了Na2CO3,碱性增强 |
| D | 光束通过Al(OH)3胶体时会发生丁达尔效应 | 胶体粒子的直径为1nm~100 nm |
查看答案和解析>>
科目:高中化学 来源: 题型:
关于下列各装置图的叙述中,不正确的是:

A.装置①中,c为阳极、d为阴极
B.装置②可用于收集H2、NH3、CO2、Cl2、HCl、NO2等气体,且从a口进气
C.装置③中X若为四氯化碳,可用于吸收氨气或氯化氢,并防止倒吸
D.装置④可用于干燥、收集氨气,并吸收多余的氨气
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验的做法正确的是( )
A.分液时,分液漏斗中的上层液体应由下口倒出
B.用加热分解的方法不能区分碳酸钠和碳酸氢钠两种固体
C.配制0.100 0 mol·L-1氯化钠溶液时,将液体转移到容量瓶中需用玻璃棒引流
D.检验NH4+时,往试样中加入NaOH溶液,微热,用湿润的蓝色石蕊试纸检验逸出的气体
查看答案和解析>>
科目:高中化学 来源: 题型:
用下图所示装置进行实验,装置正确且设计合理的是

A.图①所示装置可吸收HCl气体并防止倒吸,
B.图②所示装置进行浓硫酸稀释配制稀硫酸的实验
C.图③所示装置进行用已知浓度的NaOH溶液测定盐酸浓度的实验
D.图④所示装置进行用苯萃取碘水中碘的实验,并把碘的苯溶液从漏斗上口倒出
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关叙述正确的是
A.非金属氧化物一定为酸性氧化物
B.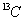 和
和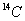 互为同位素,化学性质相似
互为同位素,化学性质相似
C.根据是否能产生丁达尔效应,将分散系分为溶液、浊液和胶体
D.已知红磷比白磷稳定,则
查看答案和解析>>
科目:高中化学 来源: 题型:
【化学——有机化学基础】
某芳香族化合物H常用作防腐剂,H可利用下列路线合成:

已知:
①A是相对分子质量为92的烃;

④D的核磁共振氢谱表明其有两种不同化学环境的氢,且峰面积之比为1:1。
回答下列问题:
(1)A的分子式为___________,由A→B的反应试剂和反应条件为____________。
(2)写出C→D的反应方程式:_________________________________________。
(3)同时符合下列条件的E的同分异构体共有____________种。
①能发生银镜反应 ②能使FeCl3溶液发生显色反应。
(4)检验F中含氧官能团的试剂为____________(填试剂名称),由F→G的反应类型为
(5)H的结构简式为_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B、C、D四块金属片,进行如下实验,①A、B用导线相连后,同时插入稀H2SO4中,A极为负极 ②C、D用导线相连后,同时浸入稀H2SO4中,电子由C→导线→D ③A、C相连后,同时浸入稀H2SO4,C极产生大量气泡 ④B、D相连后,同时浸入稀H2SO4中,D极发生氧化反应,则四种金属的活动性顺序为 ( )
A.A>B>C>D B.C>A>B>D C.A>C>D>B D.B>D>C>A
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com