
用0.1mol/L的Na2SO3溶液30mL,恰好将2×10﹣3 mol XO4﹣还原,则元素X在还原产物中的化合价是( )
|
| A. | +4 | B. | +3 | C. | +2 | D. | +1 |
科目:高中化学 来源: 题型:
烧杯中盛有液态物质A,加入少量固体物质B,B不溶解.当通入气体C时发现B逐渐溶解直至完全溶解.则A、B、C依次为()
A. H2O、BaSO4、O2 B. FeCl2溶液、Fe粉、Cl2
C. H2O、CaCO3、SO3气体 D. H2O、SiO2、HCl气体
查看答案和解析>>
科目:高中化学 来源: 题型:
要尽量除去杂质,加入的试剂必须稍过量,最后的过量物可以使用物理或化学方法除去.现要除去NaCl中少量的CaCl2、ZnCl2、Na2SO4杂质,下列选用试剂及其使用顺序正确的是()
A. Na2CO3、BaCl2、HCl B. BaCl2、Na2CO3、H2SO4
C. BaCl2、Na2CO3、HCl D. Ba(NO3)2、Na2CO3、HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
离子方程式H++OH﹣=H2O可表示的化学反应是( )
|
| A. | 盐酸和氢氧化钡的反应 | B. | 硝酸和氢氧化镁的反应 |
|
| C. | 硫酸和氢氧化钡的反应 | D. | 盐酸和氢氧化铜反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
关于容量瓶的四种叙述:①是配制准确浓度溶液的仪器;②不宜贮存溶液;③不能用来加热;④使用之前要检查是否漏水.这些叙述中正确的是( )
|
| A. | ①②③④ | B. | ②③ | C. | ①②④ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
容量瓶是用来配制物质的量浓度的溶液的定量仪器,其上标有:①温度 ②浓度 ③容量 ④压强⑤刻度线 ⑥酸式或碱式这六项中的()
A. ②④⑥ B. ③⑤⑥ C. ①②④ D. ①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
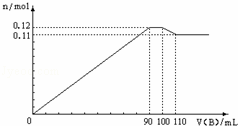
向100mLBaCl2、AlCl3、FeCl3的混合溶液A中,逐滴加入Na2SO4和NaOH的混合溶液B,产生的沉淀和加入混合溶液B的体积关系如下图所示:
(1)加入B溶液110mL时,溶液中的沉淀是 ,溶液中的溶质是 .
(2)从90mL至100mL之间加入10mL B溶液时发生的离子反应方程式是:Ba2++SO42﹣→BaSO4↓,Al(OH)3+OH﹣→AlO2﹣+2H2O溶液B中Na2SO4与NaOH的物质的量浓度之比为 ;
(3)计算A溶液中AlCl3的物质的量浓度,写出计算过程: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com