
| A. | SiC中硅元素的化合价为-4价,SiC属于共价化合物 | |
| B. | 标准状况下,22.4LCCl4中所含共价键数目为4NA | |
| C. | 该反应中CCl4是还原剂 | |
| D. | 每转移8mol电子,会生成1molSiC |
分析 该反应中Na元素化合价由0价变为+1价、C元素化合价由+4价变为-4价,所以Na是还原剂、四氯化碳是氧化剂,
A.碳的非金属性比硅的非金属性强,所以SiC中硅元素的化合价为+4价;
B.标况下,四氯化碳是液体,气体摩尔体积对其不适用;
C.四氯化碳是氧化剂;
D.根据转移电子和SiC之间的关系式计算.
解答 解:A.碳的非金属性比硅的非金属性强,所以SiC中硅元素的化合价为+4价,SiC属于共价化合物,故A错误;
B.标况下,四氯化碳是液体,气体摩尔体积不适用,所以无法计算其物质的量,导致无法计算原子个数,故B错误;
C.该反应中C元素化合价由+4价变为-4价,所以四氯化碳是氧化剂,故C错误;
D.每生成1molSiC,转移电子的物质的量=1mol×[4-(-4)]=8mol,故D正确;
故选D.
点评 本题考查氧化还原反应、分子极性判断、物质的量的计算,侧重考查基本概念、基本计算,注意气体摩尔体积适用范围及适用条件,注意C元素化合价变化,题目难度不大.


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:选择题
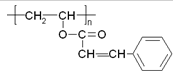 光刻胶是大规模集成电路印刷电路版技术中的关键产物,某一光刻胶的主要成分如图所示,下列有关说法正确的是( )
光刻胶是大规模集成电路印刷电路版技术中的关键产物,某一光刻胶的主要成分如图所示,下列有关说法正确的是( )| A. | 合成此高聚物的单体的化学式为C11H10O2 | |
| B. | 该物质可稳定存在于碱性溶液中 | |
| C. | 1mol该物质最多可与3molH2发生加成反应 | |
| D. | 该物质可经过缩聚反应制得 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 反应 | 大气固氮 N2(g)+O2(g)?2NO(g) | |
| 温度/℃ | 27 | 2000 |
| K | 3.84×10-31 | 0.1 |
| 容器 编号 | 起始时各物质物质的量/mol | 达平衡时体系的 能量变化 | ||
| N2 | H2 | NH3 | ||
| a | 1 | 3 | 0 | 放热23.1kJ |
| b | 0.6 | 1.8 | 0.8 | 吸热Q kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锂电池是一种质量轻、额定电压高、寿命长的高能电池 | |
| B. | 铅蓄电池可放电亦可充电,属于一次电池 | |
| C. | 燃料电池具有能量转化率高,能长时间供电等优点 | |
| D. | 原电池是利用氧化还原反应将化学能转化为电能的装置 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 高中化学教材介绍了钠、镁、铝、铁、氯、硫、氮、硅等元素及其化合物的知识,是学习研究其它化学知识的载体.
高中化学教材介绍了钠、镁、铝、铁、氯、硫、氮、硅等元素及其化合物的知识,是学习研究其它化学知识的载体.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 当一个可逆反应达到平衡状态时,这个反应的正、逆反应速率相等 | |
| B. | 化学平衡状态是一种静止状态,因为反应物和生成物的浓度已经不再改变 | |
| C. | 当一个可逆反应达到平衡状态时,就是这个反应在该条件下所能达到的最大限度 | |
| D. | 化学反应的限度不可以通过改变条件而改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 钠暴露在空气中,表面变暗,生成白色固体氧化钠 | |
| B. | 用坩埚钳夹住打磨过的镁带,在酒精灯上点燃,发出耀眼的白光,放出大量的热,产生白色固体 | |
| C. | 铜的化学性质很稳定,铜在任何条件下都不会生锈 | |
| D. | 用坩埚钳夹住铁丝在酒精灯上加热红热,迅速伸进氧气瓶中,剧烈燃烧火星四射,放出大量的热,生成红棕色的固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com