
下列叙述正确的是( )
A.乙酸的酸性比碳酸强,所以它可以跟碳酸盐溶液反应,产生CO2气体
B.乙酸酸性较弱,不能使紫色石蕊试液变红
C.乙酸分子中含有碳氧双键,所以它能与溴发生加成反应使溴水褪色
D.酯化反应不属于取代反应
科目:高中化学 来源: 题型:
某学习小组拟设计如下图所示实验装置验证Ba(OH)2溶液和H2SO4溶液发生的是离子反应(夹持仪器略去)。
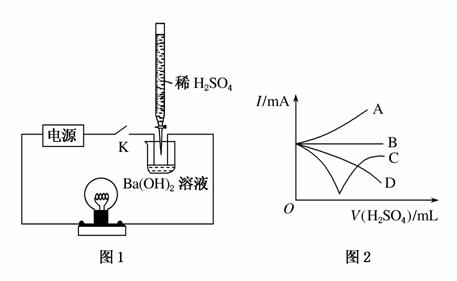
(1)该小组按图1连好装置后,接通开关K,旋转滴定管活塞使稀H2SO4缓缓滴下直至过量。图1装置中观察到的现象是______________________;能说明该反应是离子反应的依据是________。
(2)写出该反应的离子方程式____________________________。
(3)下列三种情况下,与(2)中离子方程式相同的是________。
A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO 恰好完全沉淀
恰好完全沉淀
B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性
C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量
(4)上述(1)整个过程中混合溶液的导电能力(用电流强度I表示)可近似地用图2中的________曲线表示。(填曲线对应字母)
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ.某兴趣小组用如图装置做了两次实验。
实验①:向甲池的Pt电极表面通氢气,发现电流计指针发生了偏转,乙池的Pt电极表面出现气泡。
实验②:向乙池的Pt电极表面通氧气,发现电流计指针也发生了偏转,且偏转方向与实验①相同,同时甲池的Pt电极表面也出现气泡。

(1)实验①,甲池通氢气的Pt电极为________极,电极反应式为__________________________。
(2)实验②,乙池通氧气的Pt电极为________极,电极反应式为__________________________。
(3)两次实验中原电池的总反应相同,总反应的离子方程式为________________________________。
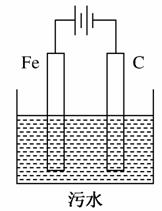
Ⅱ.电解 池污水处理技术已很成熟。富含悬浮物的工业污水采用如图装置进行处理:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3胶体,吸附部分悬浮物沉降,同时阴极产生的气泡将部分悬浮物带到水面形成浮渣层,然后滤去沉淀撇掉浮渣层。富含有机废物的生活污水也可用同样方法进行处理。污水中的有机废物能被阳极的某一产物迅速降解成二氧化碳、水等无机物。
池污水处理技术已很成熟。富含悬浮物的工业污水采用如图装置进行处理:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3胶体,吸附部分悬浮物沉降,同时阴极产生的气泡将部分悬浮物带到水面形成浮渣层,然后滤去沉淀撇掉浮渣层。富含有机废物的生活污水也可用同样方法进行处理。污水中的有机废物能被阳极的某一产物迅速降解成二氧化碳、水等无机物。
(1)电解处理过程中,若污水中离子浓度较小,导电能力较差,处理效率下降,此时可向污水中加入适量的________(填选项字母)。
A.BaSO4 B.CH3COOH
C.NaNO3 D.CH3OH
(2)电解处理过程中,阳极实际发生了两个电极反应,阳极的电极反应式分别是①______________________________;②__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
水热法制备纳米颗粒Y(化合物)的反应为3Fe2++2S2O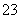 +O2+aOH-===Y+S4O
+O2+aOH-===Y+S4O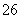 +2H2O,下列说法中,不正确的是( )
+2H2O,下列说法中,不正确的是( )
A.a=4
B.Y的化学式为Fe2O3
C.S2O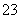 是还原剂
是还原剂
D.每有1 mol O2参加反应,转移的电子为4 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下下列各组离子在给定条件下一定能大量共存的是( )
A.水电离出的c(H+)=1×10-14 mol·L-1的溶液:K+、AlO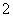 、Br-、Cl-
、Br-、Cl-
B.在含有Al3+、Cl-的溶液中:HCO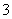 、I-、NH
、I-、NH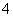 、Mg2+
、Mg2+
C.在c(H+)=1×10-13 mol·L-1的溶液中:Na+、S2-、SO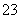 、NO
、NO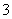
D.在溶质为KNO3和NaHSO4的溶液中:Fe2+、Ca2+、Al3+、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
人剧烈运动,骨骼肌组织会供氧不足,导致葡萄糖无氧氧化,产生大量酸性物质(分子式为C3H6O3),如果该物质过度堆积于腿部,会引起肌肉酸痛。体现该物质酸性的基团是( )
A.羟基 B.甲基
C.乙基 D.羧基
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质的分子组成符合通式CnH2nO2的是( )
①乙醇 ②乙酸 ③乙酸乙酯 ④硬脂酸 ⑤硬脂酸甘油酯
A.①②③ B.②③④
C.③④⑤ D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
茶叶中铁元素的检验可经以下四个步骤完成,各步骤中选用的实验用品不能都用到的是( )
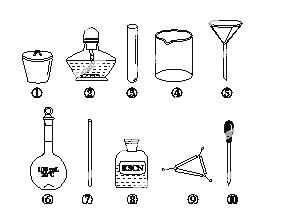
A.将茶叶灼烧灰化,选用①、②和⑨
B.用浓硝酸溶解茶叶并加蒸馏水稀释,选用④、⑥和⑦
C.过滤得到滤液,选用④、⑤和⑦
D.检验滤液中的Fe3+,选用③、⑧和⑩
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ、德国化学家凯库勒认为苯分子的结构中,碳碳间以单、双键交替结合而成环状。为了评价
凯库勒的观点,某学 生设计了以下实验方案:①按下图所示的装置图连接好各仪器;②检验装置的气密性;
生设计了以下实验方案:①按下图所示的装置图连接好各仪器;②检验装置的气密性;
③在A中加入适量的苯和液溴的混合液体,再加入少量铁粉,塞上橡皮塞,打开K1、K2、K3止水夹;④待
烧瓶C中气体收集满后,将导管D的下端插入烧杯里的水中,关闭K2,打开K3,挤压预先装有水的胶头滴
管的胶头,观察实验现象。

试回答:
(1)写出A中发生反应的化学方程式 ;能证明凯库勒观点错误的实验现象是 ;
(2)装置B的作用是 ;
Ⅱ、用中和滴定法测定烧碱的纯度,若烧碱中不含有与酸反应的杂质,试根据实验回答:
(1)准确称取烧碱样品5.0g,将样品配成25
 0mL的待测液。
0mL的待测液。
(2)取10.00mL待测液,用 量取注入锥形瓶中。(填仪器)
(3)用0.2000mol/L标准盐酸溶液滴定待测烧碱溶液,滴定时左手旋转酸式滴定管的玻璃活塞,右手不停地摇动锥形瓶,两眼注视 ,直到滴定终点。
(4)根据下列测定数据,分析得到合理数据,计算待测烧碱溶液的浓度: 。
| 滴定次数 | 待测液体积/mL | 标准盐酸体积/mL | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 10.00 | 0.50 | 20.40 |
| 第二次 | 10.00 | 4.00 | 24.10 |
| 第三次 | 10.00 | 4.20 | 25.70 |
(5)根据上述测定数据,分析得到合理数据,计算烧碱的纯度 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com