
分析 某种烃与H21:1加成得到如图所示烷烃,则该烃分子中含有1个碳碳双键,根据加成原理采取逆推法还原C=C双键,烷烃分子中相邻碳原子上均带氢原子的碳原子间是对应烯烃存在碳碳双键的位置.还原双键时注意:先判断该烃结构是否对称,如果对称,只考虑该分子一边的结构和对称线两边相邻碳原子即可;如果不对称,要全部考虑,然后各去掉相邻碳原子上的一个氢原子形成双键.
解答 解:烯烃与H21:1加成得到2-甲基丁烷,则该烃分子中含有1个碳碳双键,根据烯烃与H2加成反应的原理,推知该烷烃分子中相邻碳原子上均带氢原子的碳原子间是对应烯烃存在碳碳双键的位置,可能的结构简式为:CH2=CH-CH(CH3)2、CH3-CH=C(CH3)2、CH3-CH2-C(CH3)=CH2,命名分别为:3-甲基-1-丁烯、2-甲基-2-丁烯、2-甲基-1-丁烯;故答案为:CH2=CH-CH(CH3)2;CH3-CH=C(CH3)2;CH3-CH2-C(CH3)=CH2;3-甲基-1-丁烯、2-甲基-2-丁烯、2-甲基-1-丁烯.
点评 本题主要考查了同分异构体,题目难度中等,理解加成反应原理是解题的关键,采取逆推法还原C=C双键或三键,注意分析分子结构是否对称,防止重写、漏写.


 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | K Na Li | B. | Al Mg Na | C. | N O C | D. | Cl S P |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入饱和Na2CO3溶液除去乙酸乙酯中混有的乙酸 | |
| B. | 分离苯和硝基苯的混合物,可用蒸馏法 | |
| C. | 除去苯中的杂质苯酚可加入浓溴水后过滤 | |
| D. | 从粗苯甲酸中提纯苯甲酸,可用重结晶法 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将KI和FeCl3溶液在试管中混合后,加入CCl4,振荡后静置 | 下层呈紫红色 | 氧化性:Fe3+>I2 |
| B | 向稀硫酸中加入少量铁粉 | 溶液变为黄色 | 稀硫酸将Fe氧化成Fe3+ |
| C | 向盛Na2SiO3 溶液的试管中滴加1滴酚酞溶液,然后逐滴加入稀盐酸至红色接近消失时停止,静置 | 试管里出现凝胶 | 非金属性:Cl>Si |
| D | 葡萄糖溶液与新制的氢氧化铜混合加热 | 有砖红色沉淀生成 | 葡萄糖分子中有羟基 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
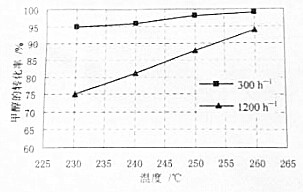 以高纯H2燃料的质子交换膜燃料电池具有能量效率高、无污染等优点,但燃料中若混有CO将显著缩短电池寿命.以甲醇为原料制取高纯H2是重要研究方向.
以高纯H2燃料的质子交换膜燃料电池具有能量效率高、无污染等优点,但燃料中若混有CO将显著缩短电池寿命.以甲醇为原料制取高纯H2是重要研究方向. 查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
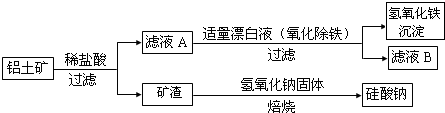
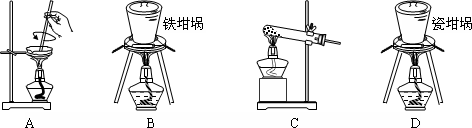
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钠和葡萄糖分别溶解在水中 | B. | 干冰和氯化铵分别受热变为气体 | ||
| C. | 食盐和冰分别受热熔化 | D. | 液溴和酒精分别挥发 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com