
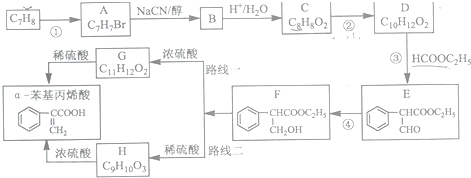


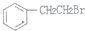 制备
制备 的合成路线.
的合成路线.分析 根据E知,C7H8为 ,反应①为取代反应,结合题给信息知,A结构简式为
,反应①为取代反应,结合题给信息知,A结构简式为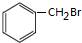 ,A发生信息①的反应,则B结构简式为
,A发生信息①的反应,则B结构简式为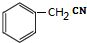 ,B发生水解反应生成C,结合C分子式知,C结构简式为
,B发生水解反应生成C,结合C分子式知,C结构简式为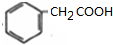 ,根据D分子式知,C发生乙醇发生酯化反应生成D,D结构简式为
,根据D分子式知,C发生乙醇发生酯化反应生成D,D结构简式为 ,D发生取代反应生成E,E发生还原反应生成F,F发生水解反应生成H,F发生消去反应生成G,G发生水解反应生成α-苯基丙烯酸,H发生消去反应生成α-苯基丙烯酸;
,D发生取代反应生成E,E发生还原反应生成F,F发生水解反应生成H,F发生消去反应生成G,G发生水解反应生成α-苯基丙烯酸,H发生消去反应生成α-苯基丙烯酸;
(7)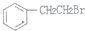 和NaOH的醇溶液加热发生消去反应生成
和NaOH的醇溶液加热发生消去反应生成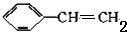 ,苯乙烯和HBr发生加成反应生成1-溴乙苯,1-溴乙苯发生取代反应,然后水解得到异苯丙酸.
,苯乙烯和HBr发生加成反应生成1-溴乙苯,1-溴乙苯发生取代反应,然后水解得到异苯丙酸.
解答 解:根据E知,C7H8为 ,反应①为取代反应,结合题给信息知,A结构简式为
,反应①为取代反应,结合题给信息知,A结构简式为 ,A发生信息①的反应,则B结构简式为
,A发生信息①的反应,则B结构简式为 ,B发生水解反应生成C,结合C分子式知,C结构简式为
,B发生水解反应生成C,结合C分子式知,C结构简式为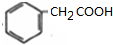 ,根据D分子式知,C发生乙醇发生酯化反应生成D,D结构简式为
,根据D分子式知,C发生乙醇发生酯化反应生成D,D结构简式为 ,D发生取代反应生成E,E发生还原反应生成F,F发生水解反应生成H,F发生消去反应生成G,G发生水解反应生成α-苯基丙烯酸,H发生消去反应生成α-苯基丙烯酸;
,D发生取代反应生成E,E发生还原反应生成F,F发生水解反应生成H,F发生消去反应生成G,G发生水解反应生成α-苯基丙烯酸,H发生消去反应生成α-苯基丙烯酸;
(1)D的结构简式为 ,故答案为:
,故答案为: ;
;
(2)反应④的反应类型是加成反应或还原反应,故答案为:加成反应或还原反应;
(3)反应所需要试剂与条件:反应①为液溴、光照,反应②为乙醇、浓硫酸、加热,
故答案为:液溴、光照;乙醇、浓硫酸、加热;
(4)D的结构简式为 ,D的同分异构体符合下列条件:
,D的同分异构体符合下列条件:
①能发生银镜反应,说明含有醛基;
②能与FeCl3溶液发生显色反应,说明含有酚羟基;
③分子中有5种不同化学环境的氢原子,
则符合条件的D的同分异构体结构简式为 ,
,
故答案为: ;
;
(5)E中含有醛基、F中不含醛基,可以用新制氢氧化铜悬浊液检验醛基,检验E是否完全转化为F的方法是取样,加入新制氢氧化铜,加热无砖红色沉淀出现,说明E已完全转化为F,
故答案为:取样,加入新制氢氧化铜,加热无砖红色沉淀出现,说明E已完全转化为F;
(6)路线二与路线一相比不太理想,理由是H既有羟基又有羧基,在浓硫酸作用下发生消去反应,会生成酯类副产物,影响产率,
故答案为:H既有羟基又有羧基,在浓硫酸作用下发生消去反应,会生成酯类副产物,影响产率;
(7)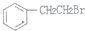 和NaOH的醇溶液加热发生消去反应生成
和NaOH的醇溶液加热发生消去反应生成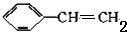 ,苯乙烯和HBr发生加成反应生成1-溴乙苯,1-溴乙苯发生取代反应,然后水解得到异苯丙酸,且合成路线为
,苯乙烯和HBr发生加成反应生成1-溴乙苯,1-溴乙苯发生取代反应,然后水解得到异苯丙酸,且合成路线为 ,
,
故答案为: .
.
点评 本题考查有机合成,为高频考点,侧重考查学生分析推断及知识综合应用能力,根据某些物质分子式、反应条件、题给信息进行推断,难点是合成路线设计,题目难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
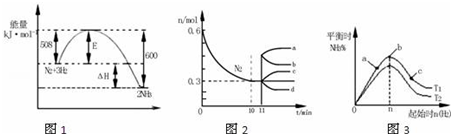
| A. | 由图1可知2NH3(g)?N2(g)+3H2(g)△H=-92kJ•mol-1 | |
| B. | 图2中0~10min内该反应的平均速率v(H2)=0.045mol•L-1•min-1,从11min起其它条件不变,压缩容器的体积为1L,则n(N2)的变化曲线为d | |
| C. | 图3中a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是b点 | |
| D. | 图3中T1和T2表示温度,对应温度下的平衡常数为K1、K2,则:T1>T2,K1>K2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该有机物分子式为 C10H10O4 | |
| B. | 1mol该有机物与 H2发生加成时最多消耗H2 5 mol | |
| C. | 1mol该有机物与足量溴水反应时最多消耗Br23 mol | |
| D. | 1mol该有机物与 NaOH 溶液反应是最多消耗NaOH 3 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
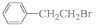 与过量NaOH醇溶液共热时发生了消去反应的是( )
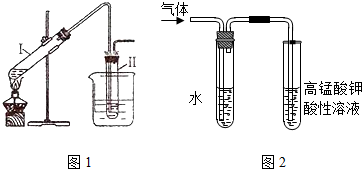
与过量NaOH醇溶液共热时发生了消去反应的是( )| A. | 混合体系$\stackrel{溴水}{→}$Br2的颜色褪去 | |
| B. | 混合体系$\stackrel{足量稀HNO_{3}}{→}$ $\stackrel{AgNO_{3}溶液}{→}$淡黄色沉淀 | |
| C. | 混合体系$\stackrel{提取}{→}$有机物$\stackrel{酸性KMnO_{4}溶液}{→}$紫色褪去 | |
| D. | 混合体系$\stackrel{提取}{→}$有机物$\stackrel{Br_{2}的CCl_{4}溶液}{→}$Br2的颜色褪去 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验现象 | 解释或结论 |
| A | 用铂丝蘸取某溶液进行焰色反应,火焰呈黄色 | 该溶液中龠Na+,不含K+ |
| B | 向某溶液中滴加KSCN溶液,无明显现象,再滴加 少量氯水,溶液变成红色 | 溶液中含有Fe2+,没有Fe3+ |
| C | 向苯中滴入少量浓溴水,振荡,精置分层,上层呈橙红色,下层几乎无色 | 苯和溴水发生取代反应,使溴水褪色 |
| D | 在少量无水乙醇中加入金属Na+,缓慢生成可以在空气中燃烧的气体 | CH3CH2OH是弱电解质 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 气态氢化物的稳定性 | B. | 最高价氧化物对应水化物的酸性 | ||
| C. | 单质与氢气反应的难易 | D. | 单质与氢气反应放出热量的多少 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
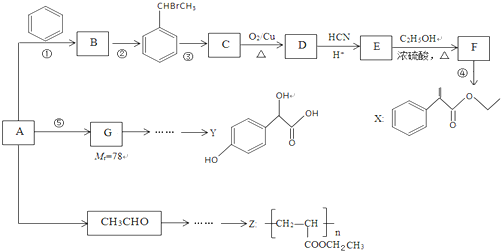
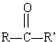 $→_{H+}^{HCN}$
$→_{H+}^{HCN}$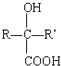 R或R′可以是烃基或氢原子
R或R′可以是烃基或氢原子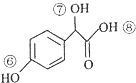 的说法正确的是AD.
的说法正确的是AD. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com