
25 ℃、101 kPa 下:①2Na(s)+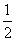 O2(g)===Na2O(s) ΔH1=-414 kJ/mol
O2(g)===Na2O(s) ΔH1=-414 kJ/mol
②2Na(s)+O2(g)===Na2O2(s) ΔH2=-511 kJ/mol。下列说法正确的是
A.①和②产物的阴阳离子个数比不相等
B.①和②生成等物质的量的产物,转移电子数不同
C.常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快
D.25 ℃、101 kPa 下,Na2O2(s)+2Na(s)===2Na2O(s) ΔH=-317 kJ/mol
科目:高中化学 来源: 题型:
下表为元素周期表的一部分,其中的序号代表对应的元素。
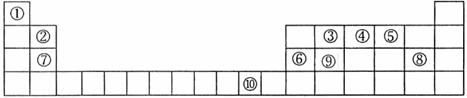
(1)在元素③与①形成的水果催熟剂气体化合物中,元素③为______杂化;根据对角线规则,②和__________性质相似(填元素符号)。
(2)元素④与元素①形成的最简单分子X中共价键键角为______。请写出一种与元素④的单质互为等电子体的分子的结构式____________。元素④的最高价氧化物的水化物的稀溶液与⑦的单质反应时,元素④被还原到最低价,该反应的化学方程式为____ ___ ___ __ __________ 。将过量的X通入含有元素⑩的硫酸盐溶液中,先沉淀后溶解,写出沉淀溶解的离子方程式__________ 。
(3) ⑥-AgO电池是应用广泛的鱼雷电池,其原理如下图所示。

该电池的负极反应式是 。
(4) ⑧(Z)和⑨(W)比较,非金属性较弱的是 (填元素符号),下列可以验证这一结论的是 (填序号)。
a.元素在地壳中的含量
 b.最高价氧化物对应水化物的酸性
b.最高价氧化物对应水化物的酸性
c.断开氢化物中1mol H—Z或H—W键所需的能量
d.Z与W以共价键形成化合物时,Z或W显示的电性
(5)钙在氧气中燃烧时得到一种钙的氧化物晶体,其晶体结构如右图所示,则该钙的氧化物的化学式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与人类生活、社会可持续发展密切相关,下列措施有利于节能减排、保护环境的是①加快化石燃料的开采与使用;②研发易降解的生物农药;③应用高效洁净的能源转换技术;④田间焚烧秸秆;⑤推广使用节能环保材料 ⑥废电池进行集中回收处理 ( )
A. ①③⑤⑥ B. ②③⑤⑥ C. ①②④ D. ②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
不久前,美国一个海军航空站安装了一 台250 kW的MCFC型燃料电池,该电池可同时供应电和水蒸气,其工作温度为600 ℃~700 ℃,所用燃料为H2,电解质为熔融的K2CO3,已知该电池的总反应为2H2+O2====2H2O, 负极反应为H2+ CO32--2e- ====H2O+CO2,则下列推断正确的是 ( )
A.正极反应为:4OH- ====O2+2H2O+4e- B.放电时CO32- 向负极移动
C.电池供应1 mol水蒸气,转移的电子数为4 mol D.放电时CO32- 向正极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
把0.4 mol X气体和0.6 mol Y气体混合于2 L密闭容器中,使它们发生如下反应:4 X(g)+5 Y(g)=n Z(g)+6 W(g)。2 min 末测得容器内的压强变为原来压强的1.05倍,且测知前2min内以Z的浓度变化表示的反应速率为0.05 mol·(L·min)-1。
求:(1)前2 min内用X的浓度变化表示的平均反应速率?
(2)2min末Y的浓度?
(3)化学反应方程式中n的值?
查看答案和解析>>
科目:高中化学 来源: 题型:
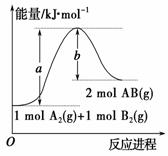
已知化学反应A2(g)+B2(g)===2AB(g)的能量变化如图所示,判断下列叙述中正确的是
A.每生成2分子AB吸收b kJ热量
B.该反应热ΔH=+(a-b)kJ·mol-1
C.该反应中反应物的总能量高于生成物的总能量
D.断裂1 mol A—A和1 mol B—B键,放出a kJ能量
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)已知:①Fe(s)+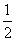 O2(g)===FeO(s) ΔH1=-272.0 kJ·mol-1;
O2(g)===FeO(s) ΔH1=-272.0 kJ·mol-1;
②2Al(s)+ O2(g)===Al2O3(s) ΔH2=-1 675.7 kJ·mol-1。
O2(g)===Al2O3(s) ΔH2=-1 675.7 kJ·mol-1。
Al和FeO发生铝热反应的热化学方程式是_____________________________某同学认为,铝热反应可用于工业炼铁,你的判断是______________(填“能”或“不能”),
你的理由是________________________________
(2)发射卫星用N2H4为燃料,NO2为氧化剂,两者反应生成N2和水蒸气, 已知N2(g)+2O2(g)=2NO2(g), 1= +67.7KJ/mol
1= +67.7KJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(l), 2 = —622KJ/mol
2 = —622KJ/mol
H2O(l) = H2O(g) ΔH3 = +44 kJ·mol-1
试写出N2H4与 NO2反应生成N2和水蒸气的热化学方程式__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
 某学生设计了一个“黑笔写红字”的趣味实验。滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹。据此,下列叙述正确的是
某学生设计了一个“黑笔写红字”的趣味实验。滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹。据此,下列叙述正确的是
A.a点是负极,b点是正极
B.铂片一端发生还原反应
C.铅笔端有少量的氯气产生
D.铅笔端作阳极
查看答案和解析>>
科目:高中化学 来源: 题型:
用 NA表示阿伏加德罗常数的值。下列说法正确的是( )
A.1 mol Na2O2晶体中共含有4NA个离子
B.0.1 mol AlCl3完全水解转化为氢氧化铝胶体,生成0.1 NA个胶粒
C.常温常压下,16 g O2和O3的混合气体中含有NA个氧原子
D.电解精炼铜时每转移NA个电子,阳极溶解32 g铜
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com