
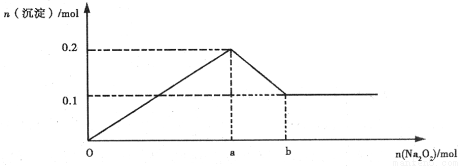
(14分)某溶液中可能含Mg2+、Al3+、Fe3+、Cu2+、NH4+、K+中的几种离子。当加入过量的过氧化钠时,有无色无味的气体产生,同时生成白色沉淀。加入的过氧化钠的量与产生沉淀的量之间的关系如图所示,试回答:
(1)该溶液中一定有 离子,一定没有 离子。
(2)无法确定是否含有 离子。要确定是否存在该离子,还需做 实验,存在该离子的实验现象为 。
(3)线段oa:ab=
(1).Mg2+ Al3+ ;Fe3+ Cu2+ NH4+ (2).K+ ;焰色反应;透过蓝色钴玻璃观察火焰为紫色
(3).5:1
【解析】
试题分析:(1)加入过氧化钠先发生的反应为:2Na2O2 + 2H2O =4 NaOH +O2↑,反应生成无色无味气体和白色沉淀,所以没有Fe3+、 Cu2+、 NH4+ ,因为Fe3+ Cu2+ 与碱生成的沉淀分别是红褐色和蓝色的,NH4+ 与NaOH生成的氨气有刺激性气味。根据图可以看出生成的沉淀有一个是不溶于NaOH 溶液,另一个可以溶于NaOH 溶液,那么Mg2+、Al3+都含有。(2)不能确定的是K+,它不与NaOH溶液反应,要确定是否有K+通常用焰色反应,所以还要做焰色反应的实验,观察K+的焰色反应颜色是要通过蓝色的钴玻璃,火焰颜色为紫色。 (3)从图看出沉淀最大值为0.2mol,最小为0.1mol,溶解的沉淀是Al(OH)3物质的量为0.1mol,,Mg(OH)2也为0.1mol,根据Mg2+ ~Mg(OH)2 Al3+~Al(OH)3要分别生成0.1mol的Mg(OH)2 和Al(OH)3共需要0.5mol的OH-,从a到b是Al(OH)3的溶解,0.1mol Al(OH)3溶解需要0.1mol 的OH-,故oa:ab=0.5mol :0.1mol=5:1。
考点:化学图像的分析、离子检验和物质的量的有关计算。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2014-2015学年甘肃省天水市高三上学期第四次检测化学试卷(解析版) 题型:选择题
下列反应的方程式正确的是
A.H2S水溶液呈酸性:H2S= H++HS-
B.醋酸钠溶液和硫酸氢钠混合:CH3COO-+H+=CH3COOH
C.向澄清石灰水中通入过量二氧化碳:Ca2++2OH-+CO2=CaCO3↓+H2O
D.碳酸钠溶液呈碱性:CO32-+2H2O=H2CO3+2OH-
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省英文学校高一上学期12月月考化学试卷(解析版) 题型:选择题
下列物质中既能跟稀H2SO4反应, 又能跟氢氧化钠溶液反应的是 ①NaHCO3 ②Al2O3③Al(OH)3 ④Al
A.③④ B.②③④ C.①③④ D.全部
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省高二上学期第三次月考化学试卷(解析版) 题型:选择题
下列电解质溶液的有关叙述正确的是
A.同浓度、同体积的强酸与强碱溶液混合后,溶液的pH=7
B.在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)增大
C.含1 mol KOH的溶液与1 mol CO2完全反应后,溶液中c(K+)= c(HCO3-)
D.在CH3COONa溶液中加入适量CH3COOH,可使c(Na+)= c(CH3COO-)
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省高二上学期第三次月考化学试卷(解析版) 题型:选择题
同一温度下,强电解质溶液a、弱电解质溶液b、金属导体c三者的导电能力相同,若升高温度后,它们的导电能力强弱顺序是
A.b>a>c B.a=b=c C.c>a>b D.b>c>a
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省高一上学期第三次考试化学试卷(解析版) 题型:选择题
某学生用NaHCO3和KHCO3组成的混合物样品与某种浓度的盐酸反应进行实验,测得数据如下表:
分析表中数据,下列说法中不正确的是

A.由①、②可知:①中的盐酸过量
B.由②、③可知:混合物的质量增加,而气体体积没有变化,说明盐酸已经反应完全
C.所用盐酸的物质的量浓度为0.4 mol·L-1
D.该混合物中NaHCO3的物质的量分数为50%
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省高一上学期第三次考试化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数,下列叙述正确的是
A.标准状况下,22.4L酒精含有的分子数为 NA
B.常温常压下,1.06g Na2CO3含有的Na+ 离子数为0.01 NA
C.11.2 L H2所含的电子数为NA
D.通常状况下,NA 个CO2分子含有原子数为3NA
查看答案和解析>>
科目:高中化学 来源:2014-2015河南省高二上学期第三次考试化学试卷(解析版) 题型:填空题
(10分)已知H2SO3是二元弱酸,常温下现有0.1 mol/L H2SO3溶液,请回答以下问题:
(1)若向H2SO3溶液中加入少量NaHSO3固体,此时溶液中c(H+)/ c(HSO3-)________(填“增大”“减小”或“不变”)。
(2)若向H2SO3溶液中加入等浓度的NaOH溶液,且二者的体积比为2∶3,若反应后溶液可使紫色石蕊变红色,则所得溶液中物料守恒式为0.1 mol/L=______________,所得溶液中各离子的物质的量浓度由大到小的顺序是__________________。
(3)若向H2SO3溶液中加入NaOH溶液至溶液恰好呈中性,此时c(Na+)______2c(SO32-)(选填“>”、“<”或“=”)。
(4)若向H2SO3溶液中加入一定量NaOH溶液,所得混合液pH=6,则此溶液中
2c(SO32-) +c(HSO3-)-c(Na+)=________mol/L。
查看答案和解析>>
科目:高中化学 来源:2014-2015甘肃省天水市高一上学期月考化学试卷(解析版) 题型:选择题
设NA表示阿伏加德罗常数的值,下列说法正确的是
A.5.6 g Fe和足量的盐酸完全反应失去电子数为0.3 NA
B.22.4L SO2含有NA个SO2分子
C.1.6g CH4所含的电子数为NA
D.标况下,4.48L的水中含有H2O分子的数目为0.2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com