
| A. | 可以用碱石灰来干燥SO2气体 | |
| B. | 通入BaCl2溶液中,能生成白色沉淀 | |
| C. | 因为SO2有漂白性,所以它能使品红溶液、溴水褪色 | |
| D. | 将SO2气体通入装有品红溶液的试管里,红色逐渐褪去,给试管加热恢复红色 |
分析 A.二氧化硫为酸性氧化物,能够与碱性物质反应;
B.亚硫酸酸性弱于盐酸,依据强酸制备弱酸规律解答;
C.依据二氧化硫漂白性、还原性解答;
D.二氧化硫具有漂白性,且其漂白性不稳定.
解答 解:A.碱石灰为碱性干燥剂,能够与二氧化硫反应,所以不能干燥二氧化硫,故A错误;
B.亚硫酸酸性弱于盐酸,依据强酸制备弱酸规律,所以二氧化硫与氯化钡溶液不反应,故B错误;
C.二氧化硫使品红褪色体现其漂白性,二氧化硫使溴水褪色体现其还原性,故C错误;
D.二氧化硫具有漂白性,且其漂白性不稳定,漂白后物质受热易恢复颜色,故D正确;
故选:D.
点评 本题考查元素化合物知识,侧重考查二氧化硫的性质,明确二氧化硫酸性氧化物、还原性、漂白性是解题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
 如图是表示:2X(g)+Y(g)?Z(g)+R(s)+Q(g)的气体反应速率(υ)与时间(t)的关系,t1时开始改变条件,则所改变的条件符合曲线的是( )
如图是表示:2X(g)+Y(g)?Z(g)+R(s)+Q(g)的气体反应速率(υ)与时间(t)的关系,t1时开始改变条件,则所改变的条件符合曲线的是( )| A. | 减少Z物质 | B. | 使用催化剂 | C. | 升高温度 | D. | 加大压强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能使酚酞试液变红的无色溶液中:Na+、CO32-、K+、ClO-、AlO2- | |
| B. | 能与金属铝反应放出氢气的溶液中:K+、SO42-、Cl-、NH4+ | |
| C. | 25℃时,某溶液中由水电离出的c(OH-)=1×10-13mol/L:NH4+、Fe3+、SO42-、Cl- | |
| D. | 含有HCO3-的溶液中:K+、OH-、NO3-、Ca2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 臭氧空洞 | B. | 酸雨 | C. | 光化学烟雾 | D. | 温室效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
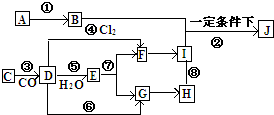 A→J有如图所示的转化关系(反应条件、部分反应物和产物已忽略):其中A、D为银白色金属单质;B为淡黄色粉末,C为红棕色粉末,E为黑色晶体;H久置于空气中,由白色固体变为灰绿色,最终变成红褐色Ⅰ;B和I在一定条件下反应生成J,J的化学式为Na2FeO4,它能够杀菌消毒,是一种优良的净水剂.
A→J有如图所示的转化关系(反应条件、部分反应物和产物已忽略):其中A、D为银白色金属单质;B为淡黄色粉末,C为红棕色粉末,E为黑色晶体;H久置于空气中,由白色固体变为灰绿色,最终变成红褐色Ⅰ;B和I在一定条件下反应生成J,J的化学式为Na2FeO4,它能够杀菌消毒,是一种优良的净水剂.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com