
分析 (1)根据盖斯定律将已知热化学方程式变形进行运算得目标方程式,焓变做相应运算求解;
(2)利用盖斯定律,将热化学方程式进行运算,(③-①+②)×$\frac{1}{2}$计算反应的焓变,得到SO3 (g)与H2O(l)反应的热化学方程式;
(3)反应为O3氧化I-生成I2,根据盖斯定律①+②+③可得总反应以及△H;
解答 解:(1)①2Ca3(PO4)2(s)+10C(s)═6CaO(s)+P4(s)+10CO(g)△H1=+3359.26kJ•mol-1
②CaO(s)+SiO2(s)═CaSiO3(s)△H2=-89.61kJ•mol-1
有盖斯定律可知,①+②×6得2Ca3(PO4)2(s)+6SiO2(s)+10C(s)═6CaSiO3(s)+P4(s)+10CO(g),
所以其反应热△H3=△H1+6×△H2=+3359.26kJ•mol-1+6×(-89.61kJ•mol-1)=+2821.6 kJ•mol-1;故答案为:+2821.6;
(2)2SO2(g)+O2(g)=2SO3(g)△H1=一197kJ/mol ①
2H2O (g)=2H2O(1)△H2=-44kJ/mol ②
2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l)△H3=一545kJ/mol③
利用盖斯定律:(③-①+②)×$\frac{1}{2}$得SO3 (g)+H2O(l)=H2SO4(l)△H=-130kJ/mol,
故答案为:SO3(g)+H2O(l)=H2SO4(l)△H=-130kJ/mol.
(3)将所给的三个反应:①+②+③可得总反应:2I-(aq)+O3(g)+2H+(aq)=I2(aq)+O2(g)+H2O(l),△H=△H1+△H2+△H3,
故答案为:2I-+O3+2H+=I2+O2+H2O;△H1+△H2+△H3;
点评 本题考查应用盖斯定律计算反应热、化学平衡常数,比较基础,注意对基础知识的理解掌握.


 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 2Cu+O2?2CuO | B. | CH4+2O2 $\frac{\underline{\;点燃\;}}{\;}$ CO2+2H2O | ||
| C. | 2KClO3?2KCl+3O2↑ | D. | CaCO3+2HCl═CaCl2+H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④>③>①>② | B. | ②>③>①=④ | C. | ②>③>①>④ | D. | ③>②>①=④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同温、同压、同体积的12C18O和14N2具有的电子数相等 | |
| B. | 同温、同压、同体积的CO和NO含有的质子数相等 | |
| C. | 同温、同压、同体积的12C18O和14N2密度不相等 | |
| D. | 同温、同压、同体积的一氧化氮(14N18O)和一氧化碳(13C18O)气体含相同的分子数和原子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2009年12月在哥本哈根召开的国际气候会议受到全球政要的广泛关注.减缓工业生产大量二氧化硫的排放以抑制全球气候变暖成为该会议的主题 | |
| B. | 针对目前甲型H1N1流感的扩散情况,要加强对环境、个人的消毒预防.其中消毒剂常选用含氯消毒剂、酒精、双氧水等适宜的物质 | |
| C. | 2009年诺贝尔物理学奖授予华裔科学家高锟,是因其在光纤材料领域取得了卓越贡献.光纤的主要成分与玛瑙相同,通常情况下不与强氧化剂和强酸反应 | |
| D. | 建国60周年庆典晚会上,天安门广场燃放的焰火是某些金属元素魅力的展现 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
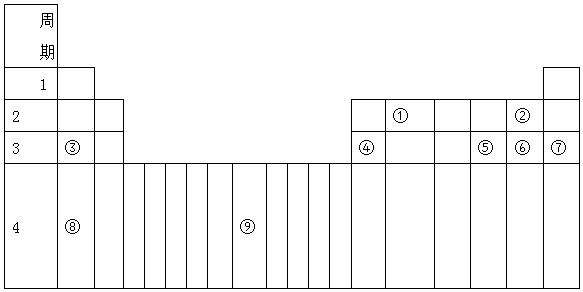
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
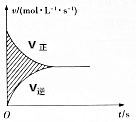 在容积为4L的刚性密闭容器中,进行可逆反应:X(g)+2Y(g)?2Z(g)并达到平衡,在此过程中以Y的浓度改变表示的反应速率v正、v逆与时间t的关系如图所示,则图中阴影部分的面积表示( )
在容积为4L的刚性密闭容器中,进行可逆反应:X(g)+2Y(g)?2Z(g)并达到平衡,在此过程中以Y的浓度改变表示的反应速率v正、v逆与时间t的关系如图所示,则图中阴影部分的面积表示( )| A. | X的浓度的变化量 | B. | Y的浓度的减小量 | ||
| C. | Z的物质的量的变化量 | D. | Y的物质的量的减小量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 全部 | B. | ①②③⑤⑥ | C. | ①③⑤⑥ | D. | ③⑤⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com