
| A£® | ClO3-µÄæռ乹ŠĶĪŖĘ½ĆęČż½ĒŠĪ | |
| B£® | ŅŅČ²·Ö×ÓÖŠµÄĮ½øöĢ¼Ō×Ó²ÉÓĆsp2ŌӻƷ½Ź½ | |
| C£® | CS2ĪŖVŠĪµÄ¼«ŠŌ·Ö×Ó | |
| D£® | SiF4ŗĶSO32-µÄÖŠŠÄŌ×Ó¾łĪŖsp3ŌÓ»Æ |
·ÖĪö A£®ĻČĒó³öÖŠŠÄŌ×ӵļŪ²ćµē×Ó¶ŌŹż£¬ŌŁÅŠ¶ĻĪ¢Į£¹¹ŠĶ£»
B£®øł¾Ż¼Ū²ćµē×Ó¶Ō»„³āĄķĀŪČ·¶ØĘäŌӻƷ½Ź½£¬¼Ū²ćµē×Ó¶ŌøöŹż=¦Ņ¼üøöŹż+¹Āµē×Ó¶ŌøöŹż£¬ĆæøöĢ¼Ō×Óŗ¬ÓŠ2øö¦Ņ¼üĒŅ²»ŗ¬¹Āµē×Ó¶Ō£¬²ÉČ”spŌӻƣ»
C£®CS2ÓėCO2·Ö×Ó¹¹ŠĶĻąĶ¬£¬øł¾Ż¶žŃõ»ÆĢ¼µÄ·Ö×Ó½į¹¹·ÖĪö£»½į¹¹¶Ō³Ę£¬ÕżøŗµēŗɵÄÖŠŠÄÖŲŗĻ£¬ŌņĪŖ·Ē¼«ŠŌ·Ö×Ó£»
D£®ĻČĒó³öÖŠŠÄŌ×ӵļŪ²ćµē×Ó¶ŌŹż£¬ŌŁÅŠ¶ĻŌÓ»ÆĄąŠĶ£¬SiF4ŗĶSO32-µÄÖŠŠÄŌ×Ó¼Ū²ćµē×Ó¶ŌŹż¶¼ĪŖ4£®
½ā“š ½ā£ŗA£®ClO3-ÖŠClµÄ¼Ū²ćµē×Ó¶ŌŹż=3+$\frac{1}{2}$£Ø7+1-2”Į3£©=4£¬ŗ¬ÓŠŅ»øö¹Āµē×Ó¶Ō£¬ŌņĄė×ÓµÄæռ乹ŠĶĪŖČż½Ē׶ŠĪ£¬¹ŹA“ķĪó£»
B£®ŅŅČ²£ØCH”ŌCH£©·Ö×ÓÖŠĆæøöCŌ×Óŗ¬ÓŠ2øö¦Ņ¼üŗĶ2øö¦Š¼ü£¬¼Ū²ćµē×Ó¶ŌøöŹżŹĒ2£¬²»ŗ¬¹Āµē×Ó¶Ō£¬ĪŖspŌӻƣ¬¹ŹB“ķĪó£»
C£®CS2ÓėCO2·Ö×Ó¹¹ŠĶĻąĶ¬£¬¶žŃõ»ÆĢ¼µÄ·Ö×Ó½į¹¹ĪŖO=C=O£¬ŌņCS2µÄ½į¹¹ĪŖS=C=S£¬ŹōÓŚÖ±ĻߊĪ·Ö×Ó£¬CS2ŗ¬ÓŠC=S¼«ŠŌ¼ü£¬·Ö×ÓĪŖĻߊĶ½į¹¹£¬½į¹¹¶Ō³Ę£¬ÕżøŗµēŗɵÄÖŠŠÄÖŲŗĻ£¬ĪŖ·Ē¼«ŠŌ·Ö×Ó£¬¹ŹC“ķĪó£»
D£®SiF4ÖŠSiµÄ¼Ū²ćµē×Ó¶ŌŹż=4+$\frac{1}{2}$£Ø4-1”Į4£©=4£¬SO32-ÖŠSµÄ¼Ū²ćµē×Ó¶ŌŹż=3+$\frac{1}{2}$£Ø6+2-2”Į3£©=4£¬ĖłŅŌÖŠŠÄŌ×Ó¾łĪŖsp3Ōӻƣ¬¹ŹDÕżČ·£®
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²é·Ö×ӵĹ¹ŠĶ”¢Ō×ÓŌӻƷ½Ź½ÅŠ¶ĻµČÖŖŹ¶µć£¬²ąÖŲæ¼²é»ł±¾ĄķĀŪ£¬ÄѵćŹĒÅŠ¶ĻŌ×ÓŌӻƷ½Ź½£¬ÖŖµĄ¹Āµē×Ó¶ŌøöŹżµÄ¼ĘĖć·½·Ø£¬ĪŖŅדķµć£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | øĆ·“Ó¦ŹĒÖĆ»»·“Ó¦ | B£® | øĆ·“Ó¦ŹĒø“·Ö½ā·“Ó¦ | ||
| C£® | CO·¢ÉśŃõ»Æ·“Ó¦ | D£® | NOŹĒ»¹Ō¼Į |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ŹµŃé²Ł×÷ | ĻÖĻó | ½įĀŪ | |
| A | ĻņijČÜŅŗÖŠĻȵĪ¼ÓĻõĖįĖį»Æ£¬ŌŁµĪ¼ÓBaCl2ČÜŅŗ | ÓŠ°×É«³ĮµķÉś³É | øĆČÜŅŗÖŠŗ¬ÓŠSO${\;}_{4}^{2-}$”¢SO${\;}_{3}^{2-}$”¢HSO${\;}_{3}^{-}$ÖŠµÄŅ»ÖÖ»ņ¼øÖÖ |
| B | ½«ÕŗÓŠÅØ°±Ė®µÄ²£Į§°ōææ½üÕŗӊijČÜŅŗµÄ²£Į§°ō | ÓŠ°×ŃĢ²śÉś | øĆČÜŅŗŹĒÅØŃĪĖį |
| C | ½«Ä³ĘųĢåĶØČėĘ·ŗģČÜŅŗÖŠ | ČÜŅŗŗģÉ«ĶŹČ„ | øĆĘųĢåæÉÄÜŹĒSO2 |
| D | ĻņijČÜŅŗÖŠµĪ¼ÓĻ”NaOHČÜŅŗŹ±£¬½«ŹŖČóµÄŗģÉ«ŹÆČļŹŌÖ½ÖĆÓŚŹŌ¹ÜæŚ | ŹŌÖ½²»±äĄ¶ | øĆČÜŅŗÖŠ²»ŗ¬NH${\;}_{4}^{+}$ |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĀČ»ÆĆ¾ | B£® | ¶žŃõ»ÆĢ¼ | C£® | ĒāĘų | D£® | ĮņĖįĶ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÖŹ×ÓÓėµē×ÓÖ®¼ä | B£® | Ė®·Ö×ÓÓėĖ®·Ö×ÓÖ®¼ä | ||
| C£® | Ńõ·Ö×ÓÖŠŃõŌ×ÓÓėŃõŌ×ÓÖ®¼ä | D£® | ĀČ»ÆÄĘÖŠÄĘĄė×ÓÓėÄĘĄė×ÓÖ®¼ä |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ”÷H3=2”÷H1+2”÷H2 | B£® | ”÷H3=2”÷H1-”÷H2 | C£® | ”÷H3=2”÷H1-2”÷H2 | D£® | ”÷H3=2”÷H1+”÷H2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Cu+HNO3£ØÅØ£©”śCu£ØNO3£©2 | |
| B£® | Cu+HNO3£ØĻ”£©”śCu£ØNO3£©2 | |
| C£® | Cu $\frac{æÕĘų}{¼ÓČČ}$ CuO $\frac{ĻõĖį}{\;}$ Cu£ØNO3£©2 | |
| D£® | Cu $\frac{ÅØĮņĖį}{¼ÓČČ}$ CuSO4 $\frac{ĻõĖį±µ}{\;}$ Cu£ØNO3£©2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
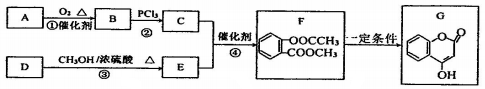
 +CH3COCl$\stackrel{“߻ƼĮ}{”ś}$
+CH3COCl$\stackrel{“߻ƼĮ}{”ś}$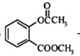 +HCl£®
+HCl£®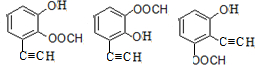 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 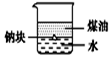 ÓĆĶ¼×°ÖĆÖ¤Ć÷¦Ń£ØĆŗÓĶ£©£¼¦Ń£ØÄĘ£©£¼¦Ń£ØĖ®£© | B£® | 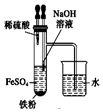 ÓĆĶ¼×°ÖĆÖʱøFe£ØOH£©2 | ||
| C£® | 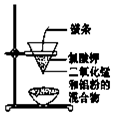 ÓĆĶ¼×°ÖĆÖĘČ”½šŹōĆĢ | D£® | 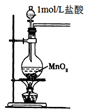 ÓĆĶ¼×°ÖĆÖĘČ”ĀČĘų |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com