
【题目】(1)已知常温时,0.1 mol/L醋酸在水中有0.1%发生电离,则该溶液的pH=__,醋酸的电离平衡常数K=__。
(2)向冰醋酸中逐滴加水,溶液导电性随加入水的体积变化如下图所示:
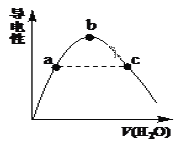
① a、b、c三点溶液中CH3COOH的电离程度由大到小的顺序是_____________。
② a、c两点对应的溶液分别吸收氨气,若两溶液最终pH均为7(25℃时),则a 点溶液中的c(CH3COO-) __c点溶液中的c(NH4+)。(填“<”、“>”或“=”)
(3)已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | Ka=1.8 | Ka1=4.3 | Ka=3.0 |
①物质的量浓度均为0.1mol/L的四种溶液:pH由小到大排列的顺序是______(用编号填写)。
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
②写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:__________。
【答案】4 10-7 c>b>a > a<d<c<b ClO﹣+H2O+CO2=HCO3﹣+HClO
【解析】
(1)0.1 mol/L醋酸在水中有0.1%发生电离,c(H+)=0.1 mol/L![]() 0.1%=10-4mol/L;
0.1%=10-4mol/L;
(2)①溶液的稀释对醋酸的电离有促进作用;
②a点为醋酸与醋酸铵形成的溶液,c点为醋酸铵溶液,两溶液导电能力相同,则产生的离子浓度相同;
(3)①四种盐为强碱弱酸盐,酸的电离平衡常数越小,酸性越弱,其钠盐水解程度越大;
②已知酸性H2CO3>HClO> HCO3﹣,则向次氯酸钠溶液中通入少量二氧化碳的产物为碳酸氢根离子。
(1)CH3COOH![]() CH3COO-+H+,0.1 mol/L醋酸在水中有0.1%发生电离,则c(H+)=0.1 mol/L
CH3COO-+H+,0.1 mol/L醋酸在水中有0.1%发生电离,则c(H+)=0.1 mol/L![]() 0.1%=10-4mol/L,pH=-lg c(H+)=4;K=c(H+)
0.1%=10-4mol/L,pH=-lg c(H+)=4;K=c(H+)![]() c(CH3COO-)/c(CH3COOH)=10-4
c(CH3COO-)/c(CH3COOH)=10-4![]() 10-4/0.1=10-7;
10-4/0.1=10-7;
(2)①溶液的稀释对醋酸的电离有促进作用,则醋酸溶液越稀,醋酸的电离程度越大,电离程度由大到小的顺序为c>b>a;
②a点为醋酸与醋酸铵形成的溶液,c点为醋酸铵溶液,两溶液导电能力相同,则产生的离子浓度相同,通入氨气时,c溶液发生H++NH3= NH4+,a溶液发生H++NH3= NH4+、CH3COOH+NH3![]() CH3COO-+NH4+,平衡正向进行,c(CH3COO-)大于c点溶液中的c(NH4+);
CH3COO-+NH4+,平衡正向进行,c(CH3COO-)大于c点溶液中的c(NH4+);
(3)①四种盐为强碱弱酸盐,酸的电离平衡常数越小,酸性越弱,其钠盐水解程度越大,溶液碱性越强,pH越大,酸性强到弱的顺序为: CH3COOH> H2CO3>HClO> HCO3-,0.1mol/L的四种溶液:pH由小到大排列的顺序为a<d<c<b;
②已知H2CO3>HClO> HCO3﹣,则向次氯酸钠溶液中通入少量二氧化碳的产物为碳酸氢根离子,离子方程式为ClO﹣+H2O+CO2=HCO3﹣+HClO。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】电—Fenton法是用于水体里有机污染物降解的高级氧化技术,其反应原理如图所示,其中电解产生的H2O2与Fe2+发生Fenton反应,Fe2++H2O2=Fe3++OH-+OH,生成的烃基自由基(OH)能氧化降解有机污染物。下列说法正确的是( )
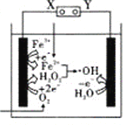
A. 电解池左边电极的电势比右边电极的电势高
B. 电解池中只有O2和Fe3+发生还原反应
C. 消耗1 molO2,电解池右边电极产生4mol OH
D. 电解池工作时,右边电极附近溶液的pH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究硫酸亚铁的分解产物,将硫酸亚铁装入下图所示的装置a中,打开K1和K2缓缓通入N2加热。实验后反应管中残留固体为红色粉末。下列说法中正确的是
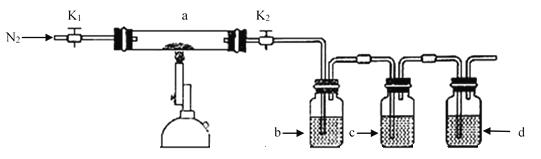
A.分解的气体产物中有SO3、SO2应该先检验SO3
B.装置b中的试剂为Ba(NO3)2溶液,反应后有白色沉淀生成,证明分解产物中有SO3气体
C.装置c中的试剂为酸性KMnO4溶液,作用是除去混合气体中的SO2
D.装置d之后需要增加尾气处理装置
查看答案和解析>>
科目:高中化学 来源: 题型:
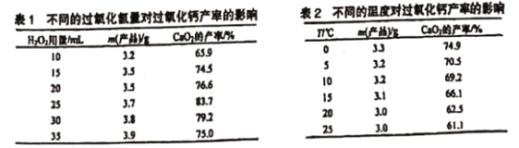
【题目】过氧化钙(CaO2)一种安全无的毒杀菌剂,以Ca(OH)2等为原料最终反应可制得CaO2。某化学研究性学习小组设计以下流程并探究不同条件对CaO2 制备的影响:
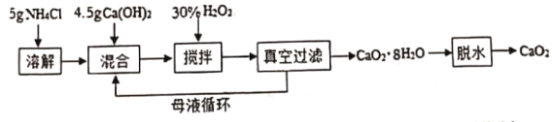
(1)搅拌过程中反应的化学反应方程式:___________________________。
(2)制备过界中除水外.可循环使用的物质是______________________。
(3)CaO2制备中H2O2合适的用量是__________________。
(4)该制备反应需控制温度在0~2℃,实验中可采取的措拖是 ___________ 。该温度下产率较高,其原因为__________________。
(5)CaO2样品中通常含有CaO,定量测定CaO2质量分数的实验方案为:_____。
(实验中可供选用的试剂有:氢氧化钠标准溶液、盐酸标准溶液、酚酞; 除常用仪器外须 使用的仪器有:电子天平、锥形瓶、滴定管)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)25 ℃时,将体积Va、pH=a的某一元强碱与体积为Vb、pH=b的某二元强酸混合。
①若所得溶液的pH=11,且a=13,b=2,则Va∶Vb=____________。
②为了更好的表示溶液的酸碱性,科学家提出了酸度(AG)的概念,AG的定义为AG=lg![]() 。25 ℃时,若溶液呈中性,则AG=___,溶液的pH与AG的换算公式为AG=_____。
。25 ℃时,若溶液呈中性,则AG=___,溶液的pH与AG的换算公式为AG=_____。
(2)常温下,浓度均为0.1molL-1的下列五种钠盐溶液的pH如下表:
溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
①上述盐溶液中的阴离子,结合H+能力最强的是____。
②根据表中数据,浓度均为0.01 molL-1的下列四种酸的溶液分别稀释100倍,pH变化最大的是__(填编号)。
A.HCN B.HClO C.CH3COOH D.H2CO3
(3)已知常温下,Ksp[Fe(OH)3]=4.0×10-38,在FeCl3溶液中加入NaHCO3溶液产生沉淀和气体,反应的离子方程式为:_______;若将所得悬浊液的pH调整为4,则溶液中Fe3+浓度为__mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一瓶无色澄清的溶液,其中可能含NH4+、K+、Na+、Mg2+、H+、Cu2+、CO32-、I-中的一种或几种,取该溶液进行如下实验:
①用PH试纸检验,表明溶液呈强酸性
②取部分溶液,加入少量的CCl4及数滴新制的氯水,振荡后CCl4层显紫色
③另取部分溶液,逐滴加入稀NaOH溶液,使溶液从酸性逐渐转变为碱性,在滴加过程中及滴加完毕后,溶液中均无沉淀生成
④将③得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。
根据上述实验事实确定并回答:
(1)在溶液中,肯定存在的有___________,肯定不存在的离子有__________________。
(2)写出实验②中的离子反应方程式________________________。
(3)不能确定是否存在的离子有__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等物质的量的X(g)与Y(g)在密闭容器中进行可逆反应:X(g)+Y(g) ![]() 2Z(g)+W(s) ΔH<0,下列叙述正确的是 ( )
2Z(g)+W(s) ΔH<0,下列叙述正确的是 ( )
A. 平衡常数K值越大,X的转化率越大
B. 达到平衡时,反应速率v正(X)=2v逆(Z)
C. 达到平衡后降低温度,正向反应速率减小的倍数大于逆向反应速率减小的倍数
D. 达到平衡后,升高温度或增大压强都有利于该反应平衡向逆反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用化学用语表示2Na+2H2O═2NaOH+H2↑中的相关微粒,其中正确的是( )
A.H2O的电子式:![]()
B.中子数为10的氧原子:![]() O
O
C.Na+的结构示意图:![]()
D.NaOH的电离方程式:NaOH═Na++O2﹣+H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上通常采用CO(g)和H2(g)催化合成甲醇CH3OH(g)。
(1)在—定温度和压强下,CO(g)+2H2(g)![]() CH3OH(g) ΔH=-128.8 kJ/mol。若将10a mol CO和20a mol H2放入2 L的密闭容器中,充分反应后测得CO的转化率为60%,则该反应的平衡常数为________(用含a的代数式表示)。若此时再向该容器中投入10a mol CO、20a mol H2和10a mol CH3OH(g),判断平衡移动的方向是________(填“正向移动”、“逆向移动”或“不移动”);与原平衡相比,CO的物质的量浓度________(填“增大”、“不变”或“减小”)。
CH3OH(g) ΔH=-128.8 kJ/mol。若将10a mol CO和20a mol H2放入2 L的密闭容器中,充分反应后测得CO的转化率为60%,则该反应的平衡常数为________(用含a的代数式表示)。若此时再向该容器中投入10a mol CO、20a mol H2和10a mol CH3OH(g),判断平衡移动的方向是________(填“正向移动”、“逆向移动”或“不移动”);与原平衡相比,CO的物质的量浓度________(填“增大”、“不变”或“减小”)。
(2)判断该反应达到平衡状态的依据是________(填字母序号)。
a.混合气体的密度不变 b.混合气体的平均相对分子质量不变 c.2v逆(H2)=v正(CO) d.容器内CO、H2、CH3OH的浓度之比为1∶2∶1 e.CH3OH、CO、H2的浓度都不再发生变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com