
| ���� | ��ɫ | �ܶȣ�g/cm3�� | �۵㣨�棩 | �е㣨�棩 | ����[KJ/kg•��] |
| Fe | ����ɫ | 7.86 | 1 535 | 2 750 | 0.44 |
| Cu | ��ɫ | 8.92 | 1 083 | 2 567 | 0.38 |
���� ��1�����ݽ������۵�ߵ��жϽ�����ʹ��������۵�͵Ľ������DZ�ʹ�ã�
��2����ѧ����ʽ��ѭԪ���غ㣬������ԭ��Ӧ�У����ϼ�����ֵ=���ϼ۽���ֵ=ת�Ƶ��������ݵ����غ�����ƽ��ѧ����ʽ��
��3�����ý�����ұ�������ǵ�ⷨ��������������Ʊ�������������Ȼ�þ��ұ������þ���ݴ˻ش�
��� �⣺��1�����ݱ������ݣ�ͭ���۵���������۵㣬Խ���۵�͵Ľ���Խ�����ױ�ұ����ʹ�õ�Խ�磬������������ʹ�õĽ���������ͭ���ʴ�Ϊ��ͭ��ͭ���۵���������۵㣻
��2����ͭ�Ļ��ϼ�������2�ۣ���Ԫ�صĻ��ϼ۽�����4�ۣ����ݵ����غ㣬����ͭԪ�ص�ϵ����2���������ʵ�ϵ����1���ʴ�Ϊ����1��1��1��1����
����Ԫ�صĻ��ϼ�������3�ۣ���Ԫ�صĻ��ϼ۽�����4�ۣ�����Fe��ϵ����4������ǰ��ϵ����3������Ԫ���غ㣬ˮ��ϵ����2n��Fe2O3•nH2O��ϵ����2���ʴ�Ϊ��
4��3��2n��2��
��3�����ý�����ұ�������ǵ�ⷨ��������ڵ����������Ʊ�����������������Ȼ�þ��ұ������þ���ʴ�Ϊ����⣻�����Ȼ�þ����MgCl2������������������Al2O3����
���� �����漰��ѧ����ʽ����ƽ��������ұ���ȷ����֪ʶ�������ۺ�֪ʶ�Ŀ��飬�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����¶���������̼���Ʒ�Ӧ�ų�������̼��˵�����ᣨH2SiO3�������Ա�̼��ǿ | |
| B�� | �մɡ�������ˮ������������������� | |
| C�� | ʯ��Ĩǽ��ˮ����ǽ��Ӳ������ԭ������ͬ | |
| D�� | ��������Һ���ռ���Һ��������Һ��Ũ����������Һ�����ô����������Լ�ƿ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
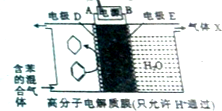
| A�� | �缫D�ĵ缫��ӦʽΪC6H6+6H++6e-=C6H12 | |
| B�� | ����X�ڷ�Ӧ��ͨ�����ֻ�ԭ�� | |
| C�� | �缫DΪ���Ե缫��EΪ���õ缫 | |
| D�� | ���·���ӵ��ƶ�����A����Դ��B |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
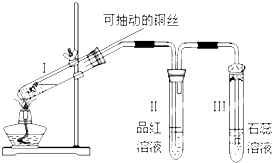
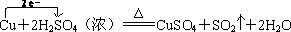 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
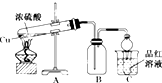 ij��ѧ��ȤС��Ϊ̽��ͭ��Ũ����ķ�Ӧ������ͼ��ʾװ�ý����й�ʵ�飮
ij��ѧ��ȤС��Ϊ̽��ͭ��Ũ����ķ�Ӧ������ͼ��ʾװ�ý����й�ʵ�飮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
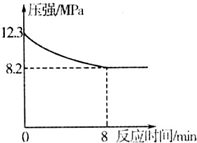 �о�̼���仯��������ʶ��ڿ��С��������������Ҫ���壮
�о�̼���仯��������ʶ��ڿ��С��������������Ҫ���壮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
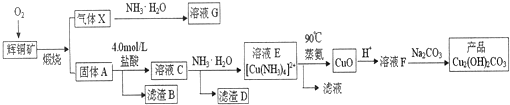
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com