
(15分)针对网络上流传的隔夜熟肉中因亚硝酸钠(NaNO2)含量严重超标而不能食用的说法,某兴趣小组开展如下探究活动:
活动一:查阅资料
NaNO2有毒,具有氧化性和还原性,NaNO2溶液显碱性,肉类在放置过程中,NaNO3逐渐转化为NaNO2,国家规定肉制品中NaNO2含量不能超过30mg/kg。
活动二:鉴别NaNO2与食盐
(1)NaNO2与食盐的外观相似,易被当成食盐误用,分析以下两种鉴别方法:
①能否各取少许固体用舌头品尝?____________。
②用稀硫酸、淀粉和KI溶液鉴别,溶液变蓝的是NaNO2具有_________性。
活动三:探究NaNO3与NaNO2的相互转化
(2)制取NaNO2与NaNO3混合溶液的装置示意图如下
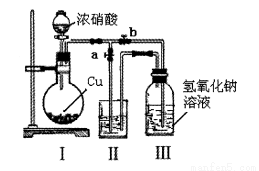
已知:2NO2+2NaOH=NaNO2+NaNO3+H2 O
①写出装置I中发生反应的化学方程式____________________________。
②水_____________(选填“能"或“不能”)作为装置II中的试剂,理由是_____________。
③装置III中反应完全后,接下来的操作是____________________________。
(3)将NaNO2与NaNO3混合溶液露置于空气,隔夜后,测得溶液的pH减小,则溶液中NaNO2的含量_____(选填“增多”、“减少"或“不变”),原因可能是____________________________(用化学方程式解释)。
活动四:检测熟肉中NaNO2含量的变化
(4)分别从1000g刚煮熟的肉和1000g隔夜熟肉中提取NaNO3与NaNO2后,配成溶液,再分别用0.00500mol/L的高锰酸钾(酸性)溶液滴定,刚煮熟的肉消耗12.00mL,隔夜肉消耗16.00mL,(已知:2MnO4一+5 NO2一+6H+=2 Mn2++5NO3一+3 H2 O)
①滴定终点的判断依据为________________________________________________。
②隔夜熟肉中NaNO2的含量是____________mg/kg。
活动五:综合其它实验和查阅资料获知,熟肉在细菌等作用下,NaNO3部分转化为NaNO2但只要保存得当,隔夜仍可食用。
(1)①不能(1分)②氧化(1分)(2)①Cu + 4HNO3(浓)=Cu(NO3)2 + 2NO2↑+ 2H2O(2分)
②不能 (1分) NO2与水反应生成NO,会污染空气(1分) ③先打开a,再关闭b (2分)
(3)减小(1分) 2NaNO2 + O2=2NaNO3 (2分)
(4)当滴入最后一滴标准液时,锥形瓶内的溶液变红,且在30秒内不褪色。(2分) 13.8 (2分)
【解析】
试题分析:(1)①任何化学药品均不能用舌头品尝。
②用稀硫酸、淀粉和KI溶液鉴别,溶液变蓝,说明反应中有碘产生,即碘化钾被氧化,这说明NaNO2具有氧化性。
(2)①装置I是铜与浓硝酸发生氧化还原反应,则发生反应的化学方程式为Cu + 4HNO3(浓)=Cu(NO3)2 + 2NO2↑+ 2H2O。
②由于NO2与水反应生成NO,会污染空气,所以水不能作为装置II中的试剂。
③NO2是大气污染物,需要利用氢氧化钠溶液吸收,防止污染空气,所以装置III中反应完全后,接下来的操作是先打开a,再关闭b。
(3)将NaNO2与NaNO3混合溶液露置于空气,隔夜后,测得溶液的pH减小,这说明部分亚硝酸钠转化为了硝酸钠,反应的方程式为2NaNO2 + O2=2NaNO3,因此溶液中NaNO2的含量减少。
(4)①酸性高锰酸钾溶液显紫红色,因此滴定终点的判断依据为当滴入最后一滴标准液时,锥形瓶内的溶液变红,且在30秒内不褪色。
②隔夜肉消耗16.00mL酸性高锰酸钾溶液,则消耗高锰酸钾的物质的量是0.016L×0.00500mol/L=0.00008mol,则根据方程式2MnO4一+5NO2一+6H+=2 Mn2++5NO3一+3H2O可知亚硝酸钠的物质的量是0.00008mol×2.5=0.0002mol,所以隔夜熟肉中NaNO2的含量是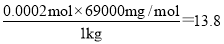 mg/kg。
mg/kg。
考点:考查亚硝酸钠性质、含量测定等实验方案设计与探究


科目:高中化学 来源:2014-2015学年江苏省镇江市高三第一学期期末调研测试化学试卷(解析版) 题型:选择题
化学与生活、生产和环境等社会实际密切相关。下列说法正确的是
A.处理废水时加入明矾作为消毒剂可以除去水中的杂质
B.利用铜、锶、钡等金属化合物的焰色反应制造节日烟花
C.高纯硅广泛应用于太阳能电池、计算机芯片和光导纤维
D.PM2.5含有的铅、镉、铬、钒、砷等元素均为对人体有害的金属元素
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省荆州市部分县市高三上学期期末统考理综化学试卷(解析版) 题型:选择题
某澄清透明溶液中只可能含有①Al3+,②Mg2+,③Fe3+,④Fe2+,⑤H+,⑥CO32-, ⑦NO3- 中的几种,向该溶液中逐滴加入NaOH溶液至过量,生成沉淀的质量与NaOH的物质的量的关系如图所示。则该溶液中一定含有的离子是
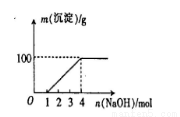
A.②⑤⑥⑦ B.②③⑤⑦
C.①②③⑥⑦ D.①②③④⑤⑦
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省唐山市高三上学期期末理综化学试卷(解析版) 题型:选择题
【化学——选修3物质结构与性质】(15分)已知A、B、C、D、E、F为前四周期的六种元素,原子序数依次增大,其中A位于周期表的s的区,其原子中电子层数和未成对电子数相同;B原子价电子排布式为nsnnpn,B和E同主族,D原子的最外层电子数是其内层的3倍;F元素位于元素周期表的第四行、第十一列。试回答下列问题:
(1)基态F原子的核外电子排布式为 。
(2)关于B2A2的下列说法中正确的是____ (填选项序号)。
①B2A2中的所有原子都满足8电子稳定结构
②每个B2A2分子中 键和
键和 键数目比为1:1
键数目比为1:1
③B2A2是由极性键和非极性键构形成的非极性分子
④B2A2中心原子的杂化类型为sp杂化
(3)B、C、D三种元素第一电离能按由大到小的顺序排列为 (用元素符号表示)。
(4)C的气态氢化物与C的最高价氧化物对应的水化物反应生成一种盐H,H晶体中存在的化学键类型
有____ (填选项序号)。
①离子键 ②共价键 ③氢键 ④配位键 ⑤金属键
(5)基态E原子的最高能层具有的原子轨道数为____ ;B和E分别与氧元素形成的最高价氧化物中,熔沸点较高的是 (写化学式);
(6)F单质的晶体堆积方式为面心立方,其配位数为 ;若F的相对分子质量为M,它的晶胞棱长为a(cm),则F晶体的密度为 g·cm-3。(阿伏伽德罗常数为NA)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省唐山市高三上学期期末理综化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数,下列叙述中正确的是
A.足量铁在氯气中反应,l mol铁失去的电子数为2 NA
B.标准状况下22.4 L H2中含中子数为2 NA
C.1 L Imol/L的盐酸溶液中,所含氯化氢分子数为NA
D.常温下46 g NO2和N2O4混合气体中含有原子数为3NA
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省泉州市高三上学期期末化学试卷(解析版) 题型:选择题
高铁酸钾(K2FeO4)是一种兼具净水和消毒功能的可溶性盐,可发生如下反应:
2K2FeO4+16HCl=4KCl+2FeCl3+8H2O+3Q↑,下列说法正确的是
A.可用湿润的淀粉碘化钾试纸检验产物Q
B.K2FeO4在水中的电离方程式为K2FeO4=2K++Fe6++4O2一
C.反应中氧化剂与还原剂的物质的量之比为1:8
D.反应中涉及的6种物质均为电解质
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省泉州市高三上学期期末化学试卷(解析版) 题型:选择题
将反应Cu(s)+2Ag+(aq)=Cu2+(aq)+2Ag(s)设计成如图所示的原电池,下列叙述正确的是
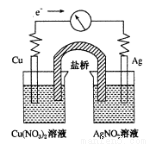
A.KNO3盐桥中的K+移向Cu(NO3)2溶液
B.Ag作负极,Cu作正极
C.工作一段时间后,Cu(NO3)2溶液中c(Cu2+)增大
D.取出盐桥后,电流计的指针依然发生偏转
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省等三校高三上学期联考化学试卷(解析版) 题型:选择题
向CuSO4溶液中逐滴加入KI溶液至过量,观察到产生白色沉淀CuI,溶液变为棕色。再向反应后的混合物中不断通人 SO2气体,溶液逐渐变成无色。下列分析正确的是
A.滴加KI溶液时,转移2 mol e-时生成 1 mol白色沉淀
B.通入SO2后溶液逐渐变成无色,体现了 SO2的漂白性
C.通入SO2时,SO2与I2反应,I2作还原剂
D.上述实验条件下,物质的氧化性:Cu2+ >I2 > SO2
查看答案和解析>>
科目:高中化学 来源:2014-2015湖北省咸宁市高一上学期期末考试化学(B)试卷(解析版) 题型:填空题
向含2 mol H2SO4和1 mol HNO3的混合稀溶液中加入过量的锌,假设HNO3被还原的产物全部为NO。
①写出反应的离子方程式 。
②生成的气体在标况下的体积为: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com