
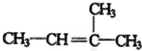 的名称是
的名称是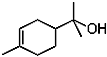 的分子式是
的分子式是
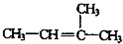 分子中含有一个碳碳双键,编号从距离双键最近且甲基编号最小一端开始,命名为:2-甲基-2-丁烯;
分子中含有一个碳碳双键,编号从距离双键最近且甲基编号最小一端开始,命名为:2-甲基-2-丁烯;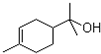 分子中,含有10个C原子,18个氢原子,一个氧原子,分子式为:C10H18O;手性碳原子指连有四个不同基团的碳原子,满足的条件的只有一个C原子,即苯环上的右边与取代基相连的碳原子为手性碳原子,
分子中,含有10个C原子,18个氢原子,一个氧原子,分子式为:C10H18O;手性碳原子指连有四个不同基团的碳原子,满足的条件的只有一个C原子,即苯环上的右边与取代基相连的碳原子为手性碳原子,

 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案科目:高中化学 来源: 题型:
| A、溶液中的c(CH3COO-) |
| B、溶液中的c(H+) |
| C、醋酸的电离平衡常数 |
| D、溶液中的c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2mol水的摩尔质量和1 mol水的摩尔质量 |
| B、200mL 1 mol/L氯化钙溶液中c(Cl-)和100 mL 1 mol/L氯化钾溶液中c(Cl-) |
| C、64g二氧化硫中的氧原子数和标准状况下22.4L二氧化碳中的氧原子数 |
| D、2mol/LBa(OH)2溶液中Ba2+的物质的量和OH-的物质的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、取样,加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- |
| B、取样,加入硝酸银有白色沉淀,一定有Cl- |
| C、取样,加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ |
| D、取样,滴加KSCN溶液,不显红色,再滴加氯水后显红色,一定有Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
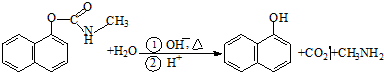
| A、西维因是一种芳香烃 |
| B、西维因分子中所有碳原子一定共面 |
| C、可用FeCl3溶液检验西维因是否发生水解 |
| D、在Ni催化下1mol西维因最多能与6molH2加成 |
查看答案和解析>>
科目:高中化学 来源: 题型:

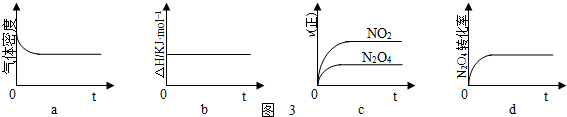
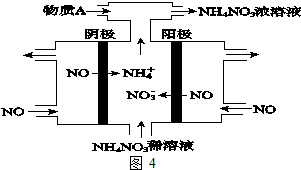
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | 颜色、性质 | 物质 | 颜色、性质 | |
| 氢氧化铜Cu(OH)2 | 蓝色固体不溶于水 | 硫酸铜(CuSO4) | 溶液呈蓝色 | |
| 氧化亚铜(Cu2O) | 红色固体不溶于水 | 氯化铜(CuCl2) | 溶液呈绿色,稀溶液呈蓝色 | |
| 氯化亚铜(CuCl) | 白色固体不溶于水 | 碱式氯化铜 | 绿色固体不溶于水 |
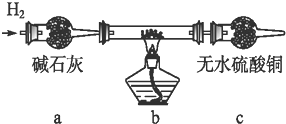 实验结束后,碳棒上的白色物质变为红色,无水硫酸铜不变色.
实验结束后,碳棒上的白色物质变为红色,无水硫酸铜不变色.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2NO2?N2O4 (正反应为放热反应) |
| B、C(s)+CO2?2CO (正反应为吸热反应) |
| C、N2+3H2?2NH3 (正反应为放热反应) |
| D、H2S?H2+S(s)(正反应为吸热反应) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com