
【题目】X、Y、Z、W、U五种元素,均位于周期表的前四周期,它们的核电荷数依次增加,且核电荷数之和为54。X的激发态原子电子排布式为2p1,Y原子的基态原子有3个不同的能级,且各能级中电子数相等,Z的基态原子中有3个未成对电子,W的电离能如下表所示,U原子的K层电子数与最外层电子数之比为2:1,其d轨道处于全充满状态。
元素 | 第一电离能 | 第二电离能 | 第三电离能 |
W | 495.8 | 4562 | 6910.3 |
(1)U原子电子排布式为_______________。
(2)X与Z 形成的化合物Z2X4,Z原子采取的杂化轨道类型为_______,Y的最高价氧化物的水化物的正盐的阴离子的空间构型为_______;
(3)W的氯化物和Mg的氯化物中,熔点较高的是________(填化学式),原因是_______。
(4)I4O9由一种阳离子和一种阴离子按物质的量比1:3构成,阴离子的空间构型为三角锥形,中心原子杂化类型为sp3杂化,写出I4O9的电离方程式______。
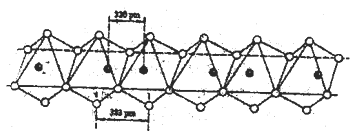
(5)Nb(黑球)和I(白球)能形成一种线性的无机高分子化合物,其结构是许多八面体通过棱边而联结起来的长链,如下图所示。则该化合物中Nb和I的原子个数比为______。
【答案】 1s22s22p63s23p63d104s1 sp3 平面三角形 MgCl2 NaCl和MgCl2都为离子晶体,Mg2+半径小,电荷数大,因此MgCl2晶体的晶格能大,熔点高 I4O9=I3++3IO3- 1:4
【解析】X、Y、Z、W、U五种元素,均位于周期表的前四周期,它们的核电荷数依次增加,且核电荷数之和为54。X的激发态原子电子排布式为2p1,X是H;Y原子的基态原子有3个不同的能级,且各能级中电子数相等,Y是C;Z的基态原子中有3个未成对电子,Z是N;W的第二电离能远大于第一电离能,所以W是第ⅠA元素,W是Na,U原子的K层电子数与最外层电子数之比为2:1,其d轨道处于全充满状态,所以U是铜。则
(1)铜的原子序数是29,原子电子排布式为1s22s22p63s23p63d104s1。(2)X与Z形成的化合物N2H4的分子中N原子的价层电子对数是4,含有一对孤对电子,则N原子采取的杂化轨道类型为sp3;C的最高价氧化物的水化物的正盐的阴离子CO32-中C原子的价层电子对数是3,不存在孤对电子,其空间构型为平面三角形;(3)由于NaCl和MgCl2都为离子晶体,Mg2+半径小,电荷数大,因此MgCl2晶体的晶格能大,熔点高;(4)I4O9由一种阳离子和一种阴离子按物质的量比1:3构成,阴离子的空间构型为三角锥形,中心原子杂化类型为sp3杂化,所以阴离子是IO3-,则阳离子是I3+,因此I4O9的电离方程式为I4O9=I3++3IO3-。(5)根据晶胞结构可知一个正八面体中含有1个Nb,I原子个数是2+4×1/2=4,所以该化合物中Nb和I的原子个数比为1:4。


科目:高中化学 来源: 题型:
【题目】某无色溶液可能由![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 中的若干种组成。为了确定该溶液的成分, 进行如下实验:
中的若干种组成。为了确定该溶液的成分, 进行如下实验:
① 取少量该溶液加入过量稀盐酸,有气体生成,得到甲溶液;
② 取少量甲溶液,向其中加入硝酸酸化的硝酸银溶液,出现白色沉淀甲;
③ 取少量原溶液,向其中加人Ba(OH)2溶液,出现白色沉淀乙。
根据上述实验回答下列问题:
(1)溶液中一定不存在的离子是___________________;
(2)—定存在的离子是______________________;
(3)沉淀乙中一定含有_______________________ ,可能含有________________________;
判断乙成分的方法是______________________________________________;
有关反应的离子方程式____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】奥运会篮球比赛用球男女有别。男子篮球比赛用7#球,内部空间体积大约是7.35 L,比赛时内部压强约为170 kPa。己知,在25℃,100 kPa时,气体摩尔体积约为24.5 L/mol。假设比赛场馆温度为25℃,下列说法中正确的是
A.比赛时,篮球内一般充填氮气
B.比赛时,篮球内约有空气0.3 mol
C.比赛时,篮球内约有空气14.8 g
D.当25℃,170kPa时,Vm>24.5 L/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在常温常压下,将三个分别盛满氨气、氯化氢与空气体积比为3∶1的混合气、二氧化氮的等容积烧瓶,再分别倒置于盛水的水槽中,当水进入烧瓶中,并使气体充分溶解后,假定烧瓶中溶液无损失,所得溶液的物质的量浓度之比为
A.1∶1∶1 B.5∶5∶4 C.1∶2∶3 D.1∶1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制250 mL 0.10 mol·L-1的NaOH溶液时,下列实验操作会使配得的溶液浓度偏大的是
A. 转移溶液后未洗涤烧杯和玻璃棒就直接定容
B. 转移溶液时,有液体飞溅
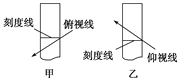
C. 在容量瓶中定容时俯视刻度线
D. 定容后把容量瓶倒转摇匀,发现液面低于刻度,再补充几滴水至刻度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物与我们的生活息息相关,下列说法正确的是( )
A.甲苯的硝化、油脂的皂化均可看作取代反应
B.蛋白质水解生成葡萄糖放出热量,提供生命活动的能量
C.石油裂解的目的是为了提高轻质液体燃料的产量和质量
D.棉花和合成纤维的主要成分是纤维素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.相对分子质量相同的几种化合物,互为同分异构体
B.分子组成相差一个或几个CH2原子团的物质,互为同系物
C.C5H11Cl的同分异构体(不考虑立体异构)共有8种
D.淀粉与纤维素是化学式为(C6H10O5)n的同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】萜类化合物广泛存在于动植物体内,关于下列萜类化合物的说法正确的是( )
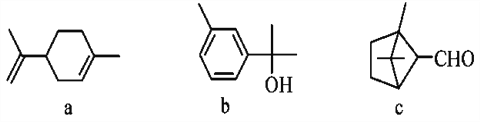
A. a和b都属于芳香族化合物
B. a和c分子中所有碳原子均处于同一平面上
C. a、b和c均能使酸性KMnO4溶液褪色
D. b和c均能与新制的Cu(OH)2反应生成红色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H是一种新型香料的主要成分之一,其合成路线如下(部分产物和部分反应条件略去):

已经:![]() 请回答下列问题:
请回答下列问题:
(1)(CH3)2C=CH2的同分异构体中存在顺反异构的有机物的名称为__________。
(2)A的核磁共振氢谱除苯环上的H外,还显示__________组峰,峰面积比为__________。
(3)D分子中含有的含氧官能团名称是__________,E的结构简式为__________。
(4) 发生加聚反应的化学方程式为______________________________;
发生加聚反应的化学方程式为______________________________;
D和G反应生成H的化学方程式为______________________________。
(5)G的同分异构体中,同时满足下列条件的有__________种(不包括立体异构)。
①苯的二取代物 ②与FeCl3溶液发生显色反应 ③含“-COO-”结构
(6)参照上述合成路线,以丙烯为原料(无机试剂任选),设计制备2,3-丁二醇的合成路线______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com