
|
ŅĄ¾ŻŅŌĻĀ·“Ó¦£ŗ ¢Ł2BrO3££«Cl2 ¢Ś5Cl2£«I2£«6H2O ¢ŪClO3££«5Cl££«6H+ ĻĀĮŠĪ¢Į£µÄŃõ»ÆŠŌĒæČõĖ³ŠņÕżČ·µÄŹĒ | |
| [””””] | |
A£® |
BrO3££¾ClO3££¾Cl2£¾IO3£ |
B£® |
BrO3££¾Cl2£¾ClO3££¾IO3£ |
C£® |
ClO3££¾BrO3££¾IO3££¾Cl2 |
D£® |
Cl2£¾BrO3££¾ClO3££¾IO3£ |

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
 ¢ń£ŗČēĶ¼±ķŹ¾800”ꏱ£¬A”¢B”¢CČżÖÖĘųĢåĪļÖŹµÄÅضČĖꏱ¼äµÄ±ä»ÆĒéæö£¬t1ŹĒ“ļµ½Ę½ŗāדĢ¬µÄŹ±¼ä£®ŹŌ»Ų“š£ŗ
¢ń£ŗČēĶ¼±ķŹ¾800”ꏱ£¬A”¢B”¢CČżÖÖĘųĢåĪļÖŹµÄÅضČĖꏱ¼äµÄ±ä»ÆĒéæö£¬t1ŹĒ“ļµ½Ę½ŗāדĢ¬µÄŹ±¼ä£®ŹŌ»Ų“š£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
 ĪŖ¼õÉŁ½»ĶØŹĀ¹Ź£¬ŠĀ½»¹ęĆ÷Įī½ūÖ¹¾Ęŗó¼Ż³µ²¢¶Ō¾Ęŗó¼Ż³µŠŠĪŖÓčŅŌÖŲ·££®ĪŖ¼ģŃé¼ŻŹ»Ō±ŹĒ·ń¾Ęŗó¼Ż³µ£¬æɲÉÓĆµÄ¼ģŃé·½·ØÓŠ¶ąÖÖ£®»Ų“šŅŌĻĀĪŹĢā£ŗ
ĪŖ¼õÉŁ½»ĶØŹĀ¹Ź£¬ŠĀ½»¹ęĆ÷Įī½ūÖ¹¾Ęŗó¼Ż³µ²¢¶Ō¾Ęŗó¼Ż³µŠŠĪŖÓčŅŌÖŲ·££®ĪŖ¼ģŃé¼ŻŹ»Ō±ŹĒ·ń¾Ęŗó¼Ż³µ£¬æɲÉÓĆµÄ¼ģŃé·½·ØÓŠ¶ąÖÖ£®»Ų“šŅŌĻĀĪŹĢā£ŗ| 56vc |
| a |
| 56vc |
| a |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
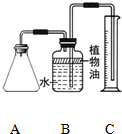 Š”Ć÷ĀņĮĖŅ»ÖÖ”°ĘūÅŻĖ¬”±µÄ³åµ÷ŅūĮĻ£®
Š”Ć÷ĀņĮĖŅ»ÖÖ”°ĘūÅŻĖ¬”±µÄ³åµ÷ŅūĮĻ£®| ŹµŃéŠņŗÅ | ¼ÓČėĖ®µÄĢå»ż | ¼ÓČėĖ®µÄĪĀ¶Č | ŹÕ¼Æµ½µÄĘųĢåµÄĢå»ż |
| 1 | 200mL | 15”ę | a£Ø“ż¼ĒĀ¼£© |
| 2 | 200 mL 200 mL |
50”ę | b£Ø“ż¼ĒĀ¼£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013½ģ¹ć¶«Ź”·šÉ½Ņ»ÖŠøßČżµŚ¶ž“Ī¶Īæ¼»ÆѧŹŌ¾ķ£Ø“ų½āĪö£© ĢāŠĶ£ŗĢīæÕĢā
£Ø13·Ö£©Ģ¼¼°Ęä»ÆŗĻĪļÓŠ¹ć·ŗµÄÓĆĶ¾”£
£Ø1£©Š“³öÓĆĢ¼°ō×÷µē¼«µē½ā±„ŗĶŹ³ŃĪĖ®µÄĄė×Ó·½³ĢŹ½£ŗ”””””””””””””” ”””””””””””””””£ £Ø2£©½«Ė®ÕōĘųĶعżŗģČȵÄĢ¼¼“æɲśÉśĖ®ĆŗĘų”£·“Ó¦ĪŖ£ŗC(s)£«H2O(g) CO(g)£«H2(g)
£Ø2£©½«Ė®ÕōĘųĶعżŗģČȵÄĢ¼¼“æɲśÉśĖ®ĆŗĘų”£·“Ó¦ĪŖ£ŗC(s)£«H2O(g) CO(g)£«H2(g)
¦¤H=" +131.3" kJ?mol-1£¬ŅŌÉĻ·“Ó¦“ļµ½Ę½ŗāŗó£¬ŌŚĢå»ż²»±äµÄĢõ¼žĻĀ£¬ŅŌĻĀ“ėŹ©ÓŠĄūÓŚĢįøßH2OµÄĘ½ŗā×Ŗ»ÆĀŹµÄŹĒ ”£
| A£®ÉżøßĪĀ¶Č”” | B£®Ōö¼ÓĢ¼µÄÓĆĮæ | C£®¼ÓČė“߻ƼĮ | D£®ÓĆCOĪüŹÕ¼Į³żČ„CO |
 £Ø3£©½«Ņ»¶ØĮæµÄCO(g)ŗĶH2O(g)·Ö±šĶØČėµ½Ģå»żĪŖ2.0LµÄŗćČŻĆܱÕČŻĘ÷ÖŠ£¬·¢ÉśŅŌĻĀ·“Ó¦£ŗCO(g)£«H2O(g) CO2(g)£«H2(g)£¬µĆµ½ČēĻĀŹż¾Ż£ŗ
£Ø3£©½«Ņ»¶ØĮæµÄCO(g)ŗĶH2O(g)·Ö±šĶØČėµ½Ģå»żĪŖ2.0LµÄŗćČŻĆܱÕČŻĘ÷ÖŠ£¬·¢ÉśŅŌĻĀ·“Ó¦£ŗCO(g)£«H2O(g) CO2(g)£«H2(g)£¬µĆµ½ČēĻĀŹż¾Ż£ŗ| ĪĀ¶Č/”ę | ĘšŹ¼Įæ/mol | Ę½ŗāĮæ/mol | “ļµ½Ę½ŗāĖł ŠčŹ±¼ä/min | ||
| H2O | CO | H2 | CO | ||
| 900 | 1.0 | 2.0 | 0.4 | 1.6 | 3.0 |
 2NH3(g) ¦¤H£½-92.4kJ?mol-1”£ŹµŃéŹŅÄ£Äā»Æ¹¤Éś²ś£¬·Ö±šŌŚ²»Ķ¬ŹµŃéĢõ¼žĻĀ·“Ó¦£¬N2ÅضČĖꏱ¼ä±ä»ÆČēĻĀĶ¼”£
2NH3(g) ¦¤H£½-92.4kJ?mol-1”£ŹµŃéŹŅÄ£Äā»Æ¹¤Éś²ś£¬·Ö±šŌŚ²»Ķ¬ŹµŃéĢõ¼žĻĀ·“Ó¦£¬N2ÅضČĖꏱ¼ä±ä»ÆČēĻĀĶ¼”£

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2010-2011ѧğ½Ī÷Ź”Ó„Ģ¶ŹŠøßČżµŚ¶ž“ĪÄ£Äāæ¼ŹŌĄķ×Ū»Æѧ²æ·Ö ĢāŠĶ£ŗĢīæÕĢā
(£±£µ·Ö)
”” ¹¤ŅµÉĻŅŌĮ×·ŹÉś²śŠĪ³ÉµÄø±²śĪļŹÆøą(CaSO4”¤2H2O)Óė½¹ĢæĪŖŌĮĻæÉÉś²śĮņĖį£¬Ķ¬Ź±æÉŅŌµĆµ½ĮņĖį¼Ų·ŹĮĻŗĶĀČ»ÆøĘĖ®ŗĻĪļ“¢ČČ²ÄĮĻ”£ŅŌĻĀŹĒÓŠ¹ŲµÄ¹¤ŅÕĮ÷³ĢŹ¾ŅāĶ¼”£
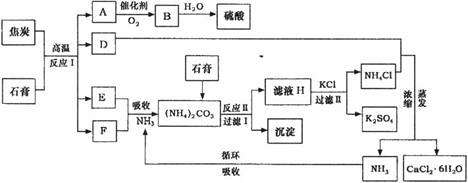
ŹŌ»Ų“š£ŗ
(1)Š“³ö·½³ĢŹ½£ŗ·“Ó¦¢ń___________________________________£¬
(2)Š“³ö·½³ĢŹ½£ŗ·“Ó¦¢ņ______________________________________”£[Ą“Ō“:ZXXK]
(3)Ēėøł¾ŻĻĀ±ķŗĶ»ÆŃ§Ę½ŗāÖŖŹ¶£¬·ÖĪö¹¤ŅµÉĻÖĘĮņĖįÖŠSO2µÄ“ß»ÆŃõ»ÆµÄŹŹŅĖĢõ¼žŹĒ
____________________________________ӣ
±ķ¢ń£ŗ
|
×Ŗ»ÆĀŹ/%
ĪĀ¶Č/”ę |
0.1 |
0.5 |
1 |
10 |
|
400 |
99.2 |
99.6 |
99.7 |
99.9 |
|
500 |
93.5 |
96.9 |
97.8 |
99.3 |
|
600 |
73.7 |
85.8 |
89.5 |
96.4 |
(4)¼ģŃéĀĖŅŗHÖŠŗ¬ÓŠCO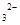 µÄ·½·ØŹĒ___________________________________”£
µÄ·½·ØŹĒ___________________________________”£
(5)ĀČ»ÆøĘ½į¾§Ė®ŗĻĪļ(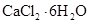 )ŹĒÄæĒ°³£ÓƵÄĪŽ»ś“¢ČČ²ÄĮĻ£¬Ń”ŌńµÄŅĄ¾ŻŹĒ___________ (ĢīŠņŗÅ)”£
)ŹĒÄæĒ°³£ÓƵÄĪŽ»ś“¢ČČ²ÄĮĻ£¬Ń”ŌńµÄŅĄ¾ŻŹĒ___________ (ĢīŠņŗÅ)”£
a£®ČŪµć½ĻµĶ(29”ęČŪ»Æ) b£®Äܵ¼µē c£®Ņ×ČÜÓŚĖ® d£®ĪŽ¶¾
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com