
某无色溶液中含有大量的H+和SO42-,则此溶液还能大量存在的离子组是
A.Na+、Fe2+、NO3- B.Na+、Mg2+、NO3-
C.Cr2O72-、Ba2+、Cl- D.K+、Na+、S2O32-
科目:高中化学 来源:2015-2016学年江西省高一下学期期末考试化学试卷(解析版) 题型:选择题
下列各图中能表示化学方程式Fe2O3+2Al 2Fe+Al2O3的是(E表示能量)( )
2Fe+Al2O3的是(E表示能量)( )
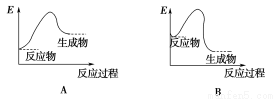
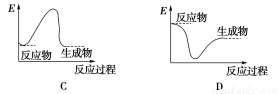
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省扬州市高二选修下学期期末调研化学试卷(解析版) 题型:选择题
常温下,下列各组离子一定能在指定溶液中大量共存的是
A.pH=1的无色溶液中: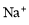 、
、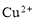 、
、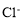 、
、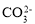
B.0.1 mol·L-1 AlCl3溶液中: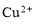 、
、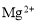 、
、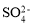 、
、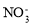
C.由水电离产生的c(H+)=10-12 mol·L-1的溶液中: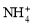 、
、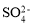 、
、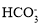 、
、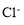
D.0.1 mol·L-1 KSCN溶液中: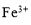 、
、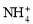 、
、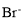 、
、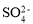
查看答案和解析>>
科目:高中化学 来源:2015-2016学年重庆一中高一下期末化学试卷(解析版) 题型:选择题
在一定条件下,容积为2L的密闭容器中,将2molM气体和3mol N气体混合,发生下列反应2M(g)+3N(g)== xQ(g)+3R(g),反应经2min达到平衡,该反应达到平衡时生成2.4molR,并测得Q浓度为0..4mol/L,下列叙述正确的是
A.X值为2
B.混合气体的密度增大
C.平衡时N的浓度为0.6mol/L
D.N的转化率为80%
查看答案和解析>>
科目:高中化学 来源:2015-2016学年重庆一中高一下期末化学试卷(解析版) 题型:选择题
短周期元素X、Y、Z、W、Q在元素周期表中的位置如表所示,其中W的气态氢化物摩尔质量为34g/mol,则下列说法中不正确的是
| X | Y |
|
Z |
| W | Q |
A.阴离子还原性:W>Q
B.X的最低价氢化物能形成分子间氢键
C.Z能在自然界中以游离态存在
D.Na与Y能形成化合物Na2Y2,1molNa2Y2与CO2反应,转移电子数为1NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年陕西西安高新一中高一下期末化学试卷(解析版) 题型:填空题
I、某学生用0.2000 mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
①用蒸馏水洗涤碱式滴定管,并注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线稍下,并记下读数
④量取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数
请回答:
(1)以上步骤有错误的是(填编号) 。
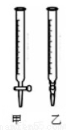
(2)用标准NaOH溶液滴定时,应将标准NaOH溶液注入______中。(从图中选填“甲”或“乙”)
(3)下列操作会引起实验结果偏大的是:______(填编号)
A.在锥形瓶装液前,留有少量蒸馏水
B.滴定前,滴定管尖嘴有气泡,滴定后无气泡
C.锥形瓶先用蒸馏水洗涤后,未用待测液润洗
D.用酸式滴定管量取液体时,释放液体前滴定管前端有气泡,之后消失
(4)滴定时,左手控制滴定管,右手摇动锥形瓶,眼睛注视 。判断到达滴定终点的现象是:锥形瓶中溶液 。
(5)以下是实验数据记录表
滴定次数 | 盐酸体积mL | NaOH溶液体积读数(mL) | |
滴定前 | 滴定后 | ||
1 | 20.00 | 0.00 | 21.30 |
2 | 20.00 | 0.00 | 16.30 |
3 | 20.00 | 0.00 | 16.32 |
通过计算可得,该盐酸浓度为:______ mol•L-1(计算结果保留4位小数)
II、利用间接酸碱滴定法可测定Ba2+的含量,实验分两步进行。
已知:2CrO42-+2H+=Cr2O72-+H2O Ba2++CrO42-=BaCrO4↓
步骤1:移取x mL一定浓度的Na2CrO4溶液于锥形瓶中,加入酸碱指示剂,用b mol·L-1盐酸标准液滴定至终点,测得滴加盐酸体积为V0 mL。
步骤2:移取y mL BaCl2溶液于锥形瓶中,加入x mL与步骤:1相同浓度的Na2CrO4溶液,待Ba2+完全沉淀后,再加入酸碱指示剂,用b mol·L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1 mL。
则BaCl2溶液浓度为______________________ mol·L-1。若步骤2中滴加盐酸时有少量待测液溅出,则Ba2+浓度的测量值将___________(填“偏大”或“偏小”)。
【答案】I、(1)①④;(2)乙;(3)B;
(4)锥形瓶内颜色;由无色变成浅红色,且半分钟内不变色。(5)0.1631;
II、(V0b-V1b)/y ;偏大。
【解析】
试题分析:(1)①根据碱式滴定管在装液前应用所装液体进行润洗,用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上,碱式滴定管未用标准氢氧化钠溶液润洗就直接注入标准NaOH溶液,标准液的浓度偏小,造成V(标准)偏大,根据c(待测)=V(标准)×c(标准) ÷V(待测),可知c(标准)偏大;④酸碱指示剂酚酞是弱电解质,也会反应消耗酸或碱,为了减少实验误差,酚酞一般滴加1滴或2滴,错误;其余操作正确;(2)NaOH是碱,容易与玻璃中的SiO2发生反应,所以应该装在碱式滴定管乙中;(3)A.在锥形瓶装液前,留有少量蒸馏水,由于不影响酸、碱的物质的量,所以对滴定操作无影响,错误;B.滴定前,滴定管尖嘴有气泡,滴定后无气泡,使标准溶液体积偏大,导致待测溶液的浓度偏高,正确;C.锥形瓶先用蒸馏水洗涤后,未用待测液润洗,操作正确,不会产生误差,错误;D.用酸式滴定管量取液体时,释放液体前滴定管前端有气泡,之后消失,则待测溶液体积偏少,反应消耗标准酸溶液的体积偏小,使测得浓度偏低,错误。(4)滴定时,左手控制滴定管,右手摇动锥形瓶,眼睛注视锥形瓶内颜色;判断到达滴定终点的现象是:锥形瓶中溶液由无色变成浅红色,且半分钟内不变色。(5)酸碱发生中和反应时二者的物质的量相等。根据实验数据可知,第一次实验数据误差太大,舍弃,V(NaOH)= (16.30+16.32)÷2=16.31mL,c(NaOH)·V(NaOH)=c(HCl)·V(HCl),所以c(HCl)=[ c(NaOH)·V(NaOH)]÷V(HCl)= [0.2000 mol·L-1×16.31mL]÷20.00mL=0.1631mol/L;II、根据方程式可知氢离子的物质的量与溶液中Ba2+的物质的量相等。步骤Ⅱ:待Ba2+完全沉淀后,再加入酸碱指示剂,用b mol•L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1 mL,则发生2CrO42-+2H+=Cr2O72-+H2O的盐酸的物质的量为:V1×10-3×bmol,步骤Ⅰ:用b mol•L-1盐酸标准液滴定至终点,测得滴加盐酸体积为V0 mL,加入的总盐酸的物质的量:V0×10-3×bmol,Ba2++CrO42-=BaCrO4↓,与Ba2+反应的CrO42-的物质的量为V0×10-3×bmol-V1×10-3×bmol=(V0 -V1)b×10-3mol,步骤Ⅱ:移取y mLBaCl2溶液于锥形瓶中,所以BaCl2溶液的浓度为:(V0 -V1)b×10-3mol ÷y×10?3mol/L=(V0b-V1b)/ymol/L;若步骤Ⅱ中滴加盐酸时有少量待测液溅出,V1减小,则Ba2+浓度测量值将偏大。
考点:考查酸碱中和滴定的有关知识。
【题型】实验题
【适用】较难
【标题】【百强校】2015-2016学年陕西西安高新一中高一下期末化学试卷(带解析)
【关键字标签】
【结束】
氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用,回答下列问题:
(1)已知:2NO2(g)  N2O(g) △H1 2NO2(g)
N2O(g) △H1 2NO2(g)  N2O(l) △H2
N2O(l) △H2
下列能量变化示意图中,正确的是(选填字母) 。

(2)氨气和氧气从145℃就开始反应,在不同温度和催化剂条件下生成不同产物(如下图)
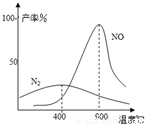
温度较低时以生成 为主,温度高于900℃时,NO产率下降的原因是 。
(3)火箭升空需要高能的燃料,经常是用四氧化二氮和联氨(N2H4)作为燃料,工业上利用氨气和氢气可以合成氨气,氨又可以进一步制备联氨等。
已知:N2(g)+2O2(g)=2NO2(g) △H=+67.7kJ•mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=-534.0kJ•mol-1
NO2(g)  1/2 N2O4(g) △H=-26.35kJ•mol-1
1/2 N2O4(g) △H=-26.35kJ•mol-1
①写出气态联氨在气态四氧化二氮中燃烧生成氮气和水蒸气的热化学方程式: 。
②用氨和次氯酸钠按一定物质的量之比混合反应可生成联氨,该反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年陕西西安高新一中高一下期末化学试卷(解析版) 题型:选择题
利用I2O5可消除CO污染,反应为I2O5(s)+5CO(g)  5CO2(g)+I2(s);不同温度下,向装有足量I2O5固体的2 L恒容密闭容器中通入2 mol CO,测得CO2气体体积分数φ(CO2)随时间t变化曲线如图所示。下列说法正确的是
5CO2(g)+I2(s);不同温度下,向装有足量I2O5固体的2 L恒容密闭容器中通入2 mol CO,测得CO2气体体积分数φ(CO2)随时间t变化曲线如图所示。下列说法正确的是

A.b点时,CO的转化率为20%
B.容器内的压强保持恒定,表明反应达到平衡状态
C.b点和d点的化学平衡常数:Kb>Kd
D.0到0.5min反应速率v(CO)=0.3 mol·L-1·min-1
【答案】C
【解析】
试题分析: A.5CO(g) +I2O5(s)  5CO2(g)+I2(s)
5CO2(g)+I2(s)
起始量/mol 2 0
转化量/mol y y
b点量/mol 2-y y
根据b点时CO2的体积分数φ(CO2)=y÷2=0.80,得y=1.6mol,转化率等于=(变化量÷起始量)×100%=(1.6÷2)×100%=80%,错误;B.两边计量数相等,所以压强始终不变,不能做平衡状态的标志,错误;C.b点比d点时生成物CO2体积分数大,说明进行的程度大,则化学平衡常数:Kb>Kd,正确;
D.0到0.5min时:5CO(g) +I2O5(s)  5CO2(g)+I2(s)
5CO2(g)+I2(s)
起始量/mol 2 0
转化量/mol x x
a点量/mol 2-x x
根据a点时CO2的体积分数φ(CO2)=x÷2=0.30,得x=0.6mol;则从反应开始至a点时的反应速率为v(CO)=(0.6mol÷2L)÷0.5min=0.6 mol·L-1·min-1,错误。
考点:考查影响化学反应速率和化学平衡影响的因素的知识。
【题型】选择题
【适用】较难
【标题】【百强校】2015-2016学年陕西西安高新一中高一下期末化学试卷(带解析)
【关键字标签】
【结束】
已知W、X、Y、Z为短周期元素,W、Z同主族,X、Y、Z同周期,W的气态氢化物的稳定性大于Z的气态氢化物的稳定性,X、Y为金属元素,X的阳离子的氧化性小于Y的阳离子的氧化性.下列说法正确的是
A. X、Y、Z、W的原子半径依次减小
B. 若W与Y的原子序数相差5,则二者形成化合物的化学式可能为Y2W3
C. W的气态氢化物的沸点一定高于Z的气态氢化物的沸点
D. W与X形成的化合物只含离子键
查看答案和解析>>
科目:高中化学 来源:2015-2016学年陕西西安高新一中高一下期末化学试卷(解析版) 题型:选择题
核磁共振(NMR)技术已广泛应用于复杂分子结构的测定和医学论断等高科技领域。已知只有质子数或中子数为奇数的原子核才有NMR现象。试判断下列哪组原子均可产生NMR现象
A. 18O、31P、119Sn
B. 元素周期表中VA族所有元素的原子
C. 27Al、19F、12C
D. 元素周期表中第一周期所有元素的原子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com