
����Ŀ��NaHSO3��Һ�ڲ�ͬ�¶��¾��ɱ�����KIO3��������NaHSO3��ȫ���ļ���I2����������I2��������ʱ��������NaHSO3�ķ�Ӧ���ʡ���Ũ�Ⱦ�Ϊ0.020 mol��L-1NaHSO3(����������)10.0 mL��KIO3(����)������Һ40.0 mL��ϣ���¼10~55������Һ����ʱ�䣬55��ʱδ�۲쵽��Һ������ʵ��������ͼ����ͼ�����������ж�����ȷ����
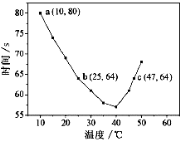
A��40��֮ǰ��40��֮����Һ������ʱ�����¶ȵı仯�����෴
B��ͼ��b��c�����Ӧ��NaHSO3��Ӧ���ʲ���
C��ͼ��a���Ӧ��NaHSO3��Ӧ����Ϊ5.0 ��10-5mol��L-1��s-1
D���¶ȸ���40��ʱ���������������������ָʾ��
���𰸡�D
��������
���������A����ͼ���п��Կ�����40����ǰ���¶�Խ�ߣ���Ӧ�ٶ�Խ�죬40�����¶�Խ�ߣ���ɫʱ��Խ������ӦԽ������55����δ������˵��û������I2����A��ȷ��B��b��ķ�Ӧԭ��Ϊ��������ع���ʱ�����ɵⵥ�ʣ������ӷ�ӦʽΪ5SO32-+2IO3-+2H+=5SO42-+I2+H2O����ͼ��c��ķ�Ӧԭ��Ϊ2IO3-+5SO2+4H2O=5SO42-+I2+8H+����Ȼͼ��b��c���Ӧ�ķ�Ӧԭ����һ�������¶�b��c���ʷ�Ӧ����b��c����B��ȷ��C��a��ʱ��Ϊ80s��Ũ�ȱ仯��Ϊ![]() =0.004mol/L��a���Ӧ��NaHSO3��Ӧ����Ϊ5.0��10-5molL-1s-1����C��ȷ��D��55��ʱ��û�г�����ɫ���ʵ����Ѳ�����Ϊ�÷�Ӧ��ָʾ������D����ѡD��
=0.004mol/L��a���Ӧ��NaHSO3��Ӧ����Ϊ5.0��10-5molL-1s-1����C��ȷ��D��55��ʱ��û�г�����ɫ���ʵ����Ѳ�����Ϊ�÷�Ӧ��ָʾ������D����ѡD��


 ��ĩ�����ϵ�д�
��ĩ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ��Cl-��Br-��I-���߸���֮����1��2��3��ͨ��һ������Cl2������Ӧ��ɺñ�ֵ��Ϊ3��2��1,��Ӧ��Cl2��ԭ��Һ��I-�ĸ���֮���ǣ� ��
A. 1��2 B. 1��3 C. 1��4 D. 1��6
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������ͻ�������Դ����������������أ������й�˵������ȷ����
A. ��ˮ�Ը߷��ӡ�ҽ������߷��ӡ�����߷��Ӿ����ڹ��ܸ߷��Ӳ���
B. ͨ�������Խ�ú�к��еı��ȷ�������ú�з������
C. ̫���ܡ��������ܡ����ܡ����ܾ���������Դ
D. �����յķ����������ֲ�˿�͵���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ�������Ա��Zn�ͼ⾧ʯ������ﮣ�ZnMn2O4��Ϊ�缫���ϣ����Ƴ�һ��ˮϵп���ӵ�ء��õ�ص��ܷ�Ӧ����ʽ��xZn +Zn1-xMn2O4![]() ZnMn2O4(0<x<1��������˵����ȷ����
ZnMn2O4(0<x<1��������˵����ȷ����
A. ZnMn2O4�Ǹ�������
B. ���ʱ��Zn2+��ZnMn2O4�缫Ǩ��
C. ���ʱ��������Ӧ��ZnMn2O4-xZn2+-2xe-=Zn1-x Mn2O4
D. ��ŵ�����У�ֻ��ZnԪ�صĻ��ϼ۷����仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. �Ҵ��Ľṹ��ʽΪC2H6O
B. ���Ӻ��Ҵ��������ǻ������ţ���������ͬһ������
C. ʵ���������������ñ���Na2CO3�ռ�
D. ϩ������̼̼˫�����ܷ���ȡ����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ʵ�����ͬ�ļ��飨CH4���Ͱ�����NH3����һ����ͬ�����ǣ� ��
A.����
B.���
C.������
D.ԭ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں��¡����������£����ܱ�ʾH2(g)��I2(g) ![]() 2HI(g)�ﵽ��ѧƽ��״̬����(����)
2HI(g)�ﵽ��ѧƽ��״̬����(����)
A. ��λʱ��������a mol H2��ͬʱ����2a mol HI
B. �����ڵ���ѹǿ����ʱ��仯
C. ������H2��I2���ټ��٣�HI��������
D. ����������ɫ���ٷ����仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�ʵ���˵����ȷ����(����)
A. ��pH��ֽ��˫��ˮ��pH
B. ����ʽ�ζ�����ȡ20.00 mL����KMnO4��Һ
C. ��������ƽ��ȡ 5.85 g NaCl����
D. �ô�ĥ�ڲ��������Լ�ƿ����Na2CO3��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���״����ӽ���Ĥȼ�ϵ���н��״�����ת��Ϊ���������ַ�Ӧԭ����
��CH3OH(g)+H2O(g)=CO2(g)+3H2(g)�� ��H= +49.0 kJ��mol��1
��CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g)����H= -192.9 kJ��mol��1
����˵����ȷ����
A. CH3OH��ȼ����Ϊ192��9 kJ��mol��1
B. ��Ӧ���е������仯��ͼ��ʾ
C. CH3OHת���H2�Ĺ���һ��Ҫ��������
D. ���ݢ���֪��Ӧ�� CH3OH(l)+1/2O2(g)=CO2(g)+2H2(g)����H>��192��9kJ��mol��1
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com