
| A、显酸性 | B、显中性 |
| C、显碱性 | D、无法确定酸碱性 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:

| A、粗盐提纯,选①和② |
| B、用CCl4提取碘水中的碘,选③ |
| C、分离Na2CO3溶液和CH3COOC2H5,选④ |
| D、用NaOH溶液吸收Cl2,选⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ba(OH)2、Na2SO3、FeCl3、KCl |
| B、Na2CO3、NaHCO3、KNO3、NH4Cl |
| C、NH3?H2O、H3PO4、Na2SO4、H2SO4 |
| D、HCl、CH3COOH、C2H5OH、Na2SiO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
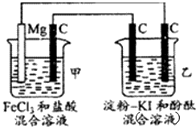
| A、甲池中Mg极为阳极,电极反应式为:Mg-2r-═Mg2+ |
| B、甲池中:当Mg减少2.4g时,石墨(C)极上产生2.24L气体 |
| C、乙池中将化学能转化为电能 |
| D、乙池左侧石墨电极附近变蓝,右侧石墨电极附近变红 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、丙烷是直链烃,所以分子中3个碳原子也在一条直线上 |
| B、丙烯所有原子均在同一平面上 |
C、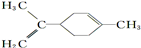 所有碳原子一定在同一平面上 所有碳原子一定在同一平面上 |
D、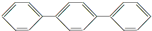 至少有16个原子共平面 至少有16个原子共平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:
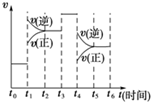 反应N2(g)+3H2(g)
反应N2(g)+3H2(g)
| ||
| △ |
| A、t0~t1 |
| B、t2~t3 |
| C、t3~t4 |
| D、t5~t6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、含有NA个氢原子的氢气在标准状况下的体积约为11.2L |
| B、25℃,1.01×105Pa,64g SO2中含有的原子数为3NA |
| C、在常温常压下,35.5g Cl2含有的分子数为0.5NA |
| D、标准状况下,11.2L H2O含有的分子数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
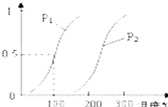 甲醇被称为2l世纪的新型燃料,工业上通过下列反应Ⅰ和Ⅱ,来制备甲醇.
甲醇被称为2l世纪的新型燃料,工业上通过下列反应Ⅰ和Ⅱ,来制备甲醇.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com