
���������һ����Ҫ����ɫ��ˮ�������о�ˮ������˫�ع��ܡ�ij����ѧϰС��������·����Ʊ�������أ�
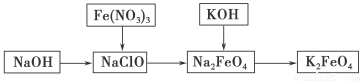
��1�������������Ԫ�صĻ��ϼ�Ϊ________���Ʋ������еĻ�ѧ������__________________��
��2�� ��֪Fe2O3��KNO3��KOH�Ļ������ȹ���Ҳ���Ƶø�����ء���ɲ���ƽ���л�ѧ����ʽ��

��3����KOH���뺬Na2FeO4����Һ�н����Сʱ�����ã����˴ֲ�Ʒ���ù��̷����ķ�ӦΪ2KOH��Na2FeO4===K2FeO4��2NaOH�����ݸ��ֽⷴӦԭ�����������Ƶ��ܽ��________(����ڡ�����С�ڡ����ڡ�)������ص��ܽ�ȡ�
��4��Ϊ�ⶨ������Һ����Ԫ�ص��ܺ�����ʵ�������
��ȷ��ȡ20.00mL������Һ�ڴ�����ƿ�У���������H2O2������ַ�Ӧ���ȳ�ȥ����H2O2��
�ڼ������KI��ַ�Ӧ��,����0.1000 mol��L-1 Na2S2O3����Һ�ζ����յ㣬���ı���Һ20.00 ml����֪��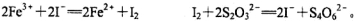
��д���ζ�ѡ�õ�ָʾ�� ,�ζ��յ�۲쵽������ ��
����Һ������Ԫ�ص��ܺ���Ϊ g��L-1�����ζ�ǰ��Һ��H2O2û�г��������ⶨ����Ԫ�صĺ������� (�ƫ�ߡ� ��ƫ�͡� �����䡱����

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016��ӱ�ʡ������ѧ�ڵ��Ĵ��¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��0.2mol/L HCN��Һ��0.1mol/L NaOH��Һ�������Ϻ���Һ�ʼ��ԣ����й�ϵʽ�в���ȷ ����
����
A. c(HCN) ��c(CN��) B. c(Na+)��c( CN��)
CN��)
C. c(HCN)��c(CN��)��c(OH��) D. c(HCN)��c(CN��)��0.1mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ����Ͽ�и�����ѧ�ڵڶ��ξ�Ӣ�Կ�����ѧ�Ծ��������棩 ���ͣ������
��֪����þ����Ҫ�ɷ�ΪMg2B2O5��H2O����ɰ�Ļ�ѧʽΪNa2B4O7��10H2O��������þ����ȡ����þ������Ĺ�������Ϊ��
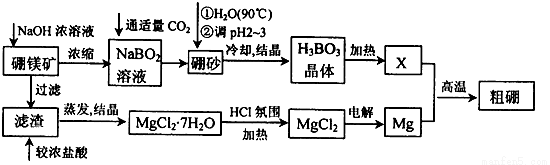
�ش������й����⣺
��1����ɰ��B�Ļ��ϼ�Ϊ ������ɰ������ˮ����ϡH2SO4��pH��2��3��ȡH3BO3���÷�Ӧ�����ӷ���ʽΪ ��
��2��MgCl2��7H2O��Ҫ��HCl��Χ�м��ȣ���Ŀ���� �����ö��Ե缫���MgCl2��Һ����������ӦʽΪ ��
��3��þ��H2O2����ȼ�ϵ�صķ�Ӧԭ��Ϊ Mg��H2O2��2H��===Mg2����2H2O�� ��������ӦʽΪ �������£�����ʼ�������ҺpH��1����pH��2ʱ����Һ��Mg2��Ũ��Ϊ______������ҺpH��6ʱ�� (��С���û�С�)Mg(OH)2��������(��֪Ksp[Mg(OH)2]��5��6��10��12)��
��4���ƵõĴ�����һ������������BI3��BI3���ȷֽ���Եõ������ĵ������ֽ�0��020 g�����Ƴɵ�BI3��ȫ�ֽ⣬���ɵ�I2��0��30 mol��L��1Na2S2O3��Һ�ζ����յ㣬����Na2S2O3��Һ18��00 mL���ô�����Ʒ�Ĵ���Ϊ____(��ʾ��I2��2S2O===2I����S4O)(�������һλС��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ�����и�����ѧ��12�½�ѧ����������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
Һ��ȼ�ϵ�����������ȼ�ϵ�ؾ������С����������洢װ�õ��ŵ㡣һ������( N2H4)Ϊȼ�ϵĵ��װ����ͼ��ʾ���õ���ÿ����е�������Ϊ��������KOH��Ϊ����ʡ����й��ڸ�ȼ�ϵ�ص���������ȷ����
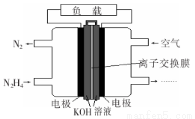
A���������Ҳ�缫�������غ��������缫
B�����������ĵ缫��ӦʽΪ��N2H4+4OH- - 4e-=N2+ 4H2O
C����ȼ�ϵ�صĵ缫����Ӧ���ö������ϣ�����ߵ缫��Ӧ�����ڵ缫���������������ʹ������������Һ��ֽӴ�
D����ȼ�ϵ�س����ŵ�ʱ��K+�Ӹ���������Ǩ�ƣ�������ӽ���Ĥ��ѡ�������ӽ���Ĥ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���Ĵ�ʡ��һ�ϵ������¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���б仯������������ԭ��Ӧ����
A��Na2SO3��Һ�ڿ����б��� B��ҵ������
C�����������Ư��ԭ�� D��������ͨ�������ʯ����Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�츣��ʡ������ѧ��12���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���й��ڽ�����ʴ����������ȷ����
A����ͭ��ͭп�Ͻ�������ͭ��ײ���ͭ��
B����������ȴ��������ױ���ʴ
C��������������ʴ�����ⸯʴ�����ڵ绯ѧ��ʴ
D��������ʴ�ı�����M - ne‑ �� Mn+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ӱ�ʡ������ѧ�ڵ��Ĵ��¿���ѧ�Ծ��������棩 ���ͣ������
��һ��������ܱ������н���ij��ѧ��Ӧ����ƽ�ⳣ������ʽΪK=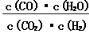 ��
��
��ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
t�� | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
�ش��������⣺
��1���÷�Ӧ�Ļ�ѧ����ʽΪ ��
��2���÷�ӦΪ ��Ӧ������ȡ����ȡ�����
��3�����жϸ÷�Ӧ�Ƿ�ﵽ��ѧƽ��״̬�������� ����ѡ�۷֣���
A��������ѹǿ���� B����������� c(CO)����
C������(H2)������(H2O) D��c(CO2)��c(CO)
��4��ij�¶��£�ƽ��Ũ�ȷ�����ʽ��c(CO2)��c(H2)��c(CO)��c(H2O)�����жϴ�ʱ���¶�Ϊ
�档
��5��ij�¶��£���CO��ˮ������1mol�������Ϊ1L���ܱ������з�Ӧ���ﵽƽ�����CO2Ϊ0.5mol����ͨ��4molˮ�������ﵽ�µ�ƽ���CO2�����ʵ�������__________mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ����Ͽ�и�����ѧ�ڵڶ��ξ�Ӣ�Կ�����ѧ�Ծ��������棩 ���ͣ�ѡ����
���л�ѧ��Ӧ�Ⱥ�˳���ж���ȷ����
A���ں��е����ʵ�����H+��Al3+����Һ�У���μ���NaOH��Һ:H+��AI3+��AI (OH )3��
B���ں��е����ʵ�����FeBr2��FeI2����Һ�У�����ͨ��������Iһ��Brһ��Fe2+
C���ں��е����ʵ�����NaCl��Na2S����Һ�м���AgNO3��Һ��NaCl��Na2S
D���ں��е����ʵ�����Fe3+��Cu2+����Һ�м������ۣ�Cu2+��Fe3+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ɽ��ʡ������ѧ��11�°��¿��Ի�ѧ�Ծ� �������棩 ���ͣ�ѡ����
�����Ը��������Һ�м���������Ʒ�ĩ����Һ��ɫ�����з�����Ӧ�����ӷ���ʽΪ��
2MnO4����16H����5Na2O2===2Mn2����5O2����8H2O��10Na���������ж���ȷ����
A��Na2O2���������������ǻ�ԭ��
B��O2�ǻ�ԭ���Mn2������������
C��ͨ����Ũ�����ữ���������Һ
D����״���£�����22.4 L O2ʱ��Ӧת��2 mol e��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com