

 ,故答案为:
,故答案为: ;
;
| ||
| ||
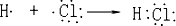 ,
,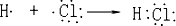 .
.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、Fe3O4可以表示为FeO?Fe2O3,则Pb3O4也可以表示为PbO?Pb2O3 |
| B、苯不可使酸性高锰酸钾溶液褪色,则甲苯也不可以使其褪色 |
| C、Si是半导体材料,则Ge也是半导体材料 |
| D、镁条在空气中燃烧生成的氧化物是MgO,则钠在空气中燃烧生成的氧化物是Na2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、生成的气体在标准状况下的体积为672 mL |
| B、生成的气体有NO和H2 |
| C、所得溶液中有溶质FeSO4和Fe2(SO4)3 |
| D、所得溶液中Fe2+的物质的量浓度为0.4 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1 mol A与足量Na反应产生2.24 L H2(标准状况) |
| B、分子式是C3H8O3 |
| C、A催化氧化的产物能发生银镜反应 |
D、A在一定条件下发生缩聚反应的产物是: |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验方案和操作 | 实验现象 | 实验结论 |
| ①将一小粒金属锂投入滴有酚酞试液的冷水中进行反应 | 锂浮在水面上,并在水面上游动,逐渐消失,溶液变为浅红色. | |
| ②将一小粒金属钠投入滴有酚酞试液的冷水中进行反应 | 钠浮在水面上,熔成一个小球,并在水面上游动,逐渐消失,溶液变为红色. | |
| ③将一小粒金属钾投入滴有酚酞试液的冷水中进行反应 | 钾浮在水面上,熔成一个光亮的小球,并在水面上快速游动,逐渐消失,溶液变为红色. | |
| ④将新制的氯水滴入溴化钾溶液中进行反应 | ||
| ⑤将溴水滴入碘化钾-淀粉溶液中进行反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、通入甲烷的一极是燃料电池的负极,该电极上发生的是还原反应 |
| B、燃料电池是将热能转换为电能的装置 |
| C、通入氧气的一极的电极反应是:O2+4e-+2H2O=4OH- |
| D、该燃料电池使用一段时间后,溶液的c(OH-)增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、它属于芳香烃 |
| B、它的分子式为C16H13ON2 |
| C、它能发生取代反应和加成反应 |
| D、它与苯互为同系物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com