
| A. | ①②③⑤ | B. | ③⑥ | C. | ③ | D. | ③⑤ |
分析 若要使平衡逆向移动,同时使c(OH-)增大,则可加入能电离出氢氧根离子的物质,结合浓度对化学平衡的影响来解答.
解答 解:①NH4Cl固体,铵根离子浓度增大,平衡逆向移动,c(OH-)减小,故错误;
②硫酸会消耗氢氧根离子,氢氧根离子浓度减小,平衡正向移动,故错误;
③NaOH固体,溶液中氢氧根离子浓度增大,电离平衡逆向移动,故正确;
④水稀释,氨水的浓度减小,平衡正向移动,氢氧根离子浓度减小,故错误;
⑤弱电解质的电离为吸热过程,加热促进电离,平衡正向移动,故错误;
⑥加入少量MgSO4固体,氢氧根离子与镁离子反应生成氢氧化镁沉淀,平衡正向移动,氢氧根离子浓度减小,故错误;
故选C.
点评 本题考查电离平衡的影响因素,注意把握浓度对电离平衡的影响为解答的关键,明确逆向移动及[OH-]增大均满足即可解答,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 2.24L | B. | 3.92L | C. | 3.36L | D. | 2.8L |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 在一定温度下,向1L体积固定的密闭容器中加入1molA(g),发生反应2A(g)?B(g)+C(g),B的物质的量随时间的变化如图所示. 0-2min内的平均反应速率v(A)=0.1mol/(L•min).相同温度下,若开始加入A(g)的物质的量是原来的2倍,则平衡时be是原来的2倍.
在一定温度下,向1L体积固定的密闭容器中加入1molA(g),发生反应2A(g)?B(g)+C(g),B的物质的量随时间的变化如图所示. 0-2min内的平均反应速率v(A)=0.1mol/(L•min).相同温度下,若开始加入A(g)的物质的量是原来的2倍,则平衡时be是原来的2倍.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (1)水的电离平衡曲线如图所示,若A点表示25℃时水的电离达平衡时的离子浓度,B点表示100℃时水的电离达平衡时的离子浓度.则100℃时1mol•L-1的NaOH溶液中,由水电离出的c(H+)=1×10-12mol•L-1.25℃时,向水的电离平衡体系中加入少量NH4Cl固体,对水的电离平衡的影响是促进(填“促进”、“抑制”或“不影响”).
(1)水的电离平衡曲线如图所示,若A点表示25℃时水的电离达平衡时的离子浓度,B点表示100℃时水的电离达平衡时的离子浓度.则100℃时1mol•L-1的NaOH溶液中,由水电离出的c(H+)=1×10-12mol•L-1.25℃时,向水的电离平衡体系中加入少量NH4Cl固体,对水的电离平衡的影响是促进(填“促进”、“抑制”或“不影响”).| 化学式 | 电离平衡常数(25℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | [HCN]<[CN-] | B. | [Na+]<[CN-] | ||
| C. | [HCN]-[CN-]=[OH-] | D. | [HCN]+[CN-]=0.1mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 微粒半径大小:S2->Cl->Na+>Al3+>F- | |
| B. | 热稳定性大小:SiH4>PH3>NH3>H2O>HF | |
| C. | 密度大小:Rb>K>Na>Li | |
| D. | 等物质的量浓度溶液,酸性强弱顺序:HClO4>H2SO4>H3PO4>H2SiO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
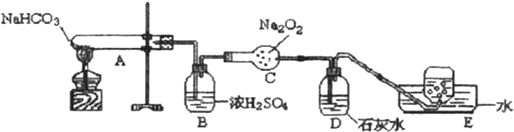
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 做焰色反应实验时,应用H2SO4清洗铂丝 | |
| B. | 焰色反应是单质特有的性质 | |
| C. | 碳酸钾在酒精灯上灼烧时能直接观察到紫色火焰 | |
| D. | NaCl与Na2SO4灼烧时火焰颜色均为黄色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com