
| A. | c(Na+)=2c(SO32-)+2c(HSO3-)+2c(H2SO3) | B. | c(Na+)+c(H+)=c(OH-)+c(SO32-)+c(HSO3-) | ||
| C. | c(OH-)=c(H+)+c(HSO3-)+2c(H2SO3) | D. | c(Na+)>c(SO32-)>c(OH-)>c(HSO3-) |
分析 A.根据亚硫酸钠溶液中的物料守恒分析;
B.亚硫酸根离子带有2个单位负电荷,则电荷守恒中其系数应该为2;
C.根据亚硫酸钠溶液中的质子守恒判断;
D.亚硫酸根离子部分水解,溶液呈碱性,由于氢氧根离子来自水的电离和亚硫酸根离子的水解,则c(OH-)>c(HSO3-).
解答 解:A.根据亚硫酸钠溶液中的物料守恒可得:c(Na+)=2c(SO32-)+2c(HSO3-)+2c(H2SO3),故A正确;
B.根据亚硫酸钠溶液中的电荷守恒可知:c(Na+)+c(H+)=c(OH-)+2c(SO32-)+c(HSO3-),故B错误;
C.亚硫酸钠溶液中满足质子守恒:c(OH-)=c(H+)+c(HSO3-)+2c(H2SO3),故C正确;
D.亚硫酸钠溶液中,亚硫酸根离子部分水解,则c(Na+)>c(SO32-),由于氢氧根离子来自水的电离和亚硫酸根离子的水解,则c(OH-)>c(HSO3-),则溶液中离子浓度大小为:c(Na+)>c(SO32-)>c(OH-)>c(HSO3-),故D正确;
故选B.
点评 本题考查了离子浓度大小比较,题目难度中等,明确盐的水解原理及其影响为解答关键,注意掌握电荷守恒、物料守恒及质子守恒的含义及应用方法,试题培养了学生的分析能力及灵活应用能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | pH HCl>CH3COOH | |
| B. | c(Cl-)=c(CH3COO-) | |
| C. | 等体积的盐酸和醋酸溶液分别与足量的Zn完全反应,盐酸产生的H2多 | |
| D. | 用同浓度的NaOH溶液分别与等体积的盐酸和醋酸溶液恰好反应完全,消耗的NaOH溶液体积一样多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2 | B. | 1 | C. | 3 | D. | 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯容易与溴的四氯化碳溶液发生反应,且1mol乙烯完全加成消耗1mol溴单质,证明乙烯分子里含有一个碳碳双键 | |
| B. | 苯分子的结构中存在碳碳单键和碳碳双键交替出现的结构 | |
| C. | 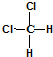 和 和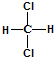 属于同一种物质,不能用来解释甲烷是一种正四面体结构 属于同一种物质,不能用来解释甲烷是一种正四面体结构 | |
| D. | 1mol CH3CH2OH与Na完全反应只生成0.5mol H2,不能说明乙醇分子中有一个氢原子与其它氢原子不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol Na2O2与足量的水反应,转移的电子数为2NA | |
| B. | 17g羟基中含有的电子数为10NA | |
| C. | 标准状况下,1mol已烷中共价键数目为19NA | |
| D. | 1L 0.10mol•L-1的Na2CO3溶液中阴离子数目之和小于0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 如图表示A、B、C、D、E五种物质的相互转化关系,其中A为淡黄色固体,C为金属单质,D为最常用的调味品.
如图表示A、B、C、D、E五种物质的相互转化关系,其中A为淡黄色固体,C为金属单质,D为最常用的调味品.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 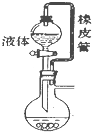 橡皮管能使液体顺利流下 | B. | 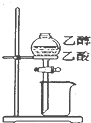 分离乙醇和乙酸 | ||
| C. | 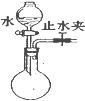 检查装置气密性 | D. | 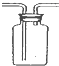 收集氨气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com