
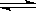 H2(g) + I2(g),达到 平衡状态的标志是
H2(g) + I2(g),达到 平衡状态的标志是 | A.I2(g)的消耗速率等于H2的消耗速率 |
| B.容器中各组分的浓度不随时间变化 |
| C.容器内气体的压强不再变化 |
| D.单位时间内生成n mol H2,同时生成n mol HI |
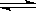 H2(g) + I2(g),达到平衡状态的标志,故A不能选;容器中各组分的浓度不随时间变化可以作为反应2HI(g)
H2(g) + I2(g),达到平衡状态的标志,故A不能选;容器中各组分的浓度不随时间变化可以作为反应2HI(g) 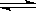 H2(g) + I2(g),达到平衡状态的标志,故B为本题的答案;反应2HI(g)
H2(g) + I2(g),达到平衡状态的标志,故B为本题的答案;反应2HI(g) 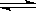 H2(g) + I2(g)的压强自始自终都是不变,不能作为反应达到平衡的标志,故C不能选;在反应开始的任何时候都是单位时间内生成n mol H2,同时生成n mol HI,所以不能作为反应达到平衡的标志,故D不能选。
H2(g) + I2(g)的压强自始自终都是不变,不能作为反应达到平衡的标志,故C不能选;在反应开始的任何时候都是单位时间内生成n mol H2,同时生成n mol HI,所以不能作为反应达到平衡的标志,故D不能选。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
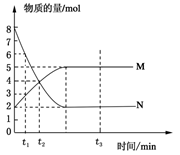
| A.t2时M与N的物质的量浓度之比为1:1 |
| B.t2与t3时刻的混合气体的平均相对分子质量相等 |
| C.反应物与生成物平衡时的物质的量浓度之比是2:5 |
D.0~t2内用M表示的平均反应速率是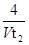 mol/(L?min) mol/(L?min) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.当某可逆反应达到平衡状态时,这就是这个反应所能达到的限度 |
| B.当某可逆反应进行到平衡状态时,这个反应的正向反应速率和逆向反应速率相等 |
| C.平衡状态是一种静止的状态,因为反应物和生成物的浓度已经不再改变 |
| D.化学反应的限度不可以通过改变条件而改变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

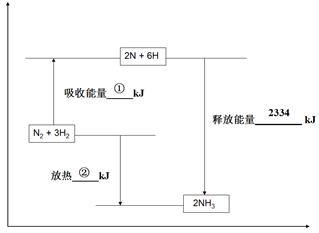
 CH3OH(g)
CH3OH(g)| 时间/浓度 | c(CO)(mol/L) | C(H2 )(mol/L) | c(CH3OH)(mol/L) |
| 起始 | 0.200 | 0.300 | 0.000 |
| 第4 min | a | b | c |
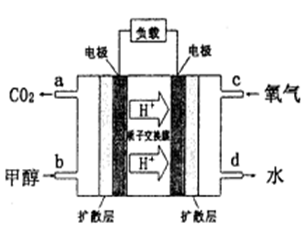
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
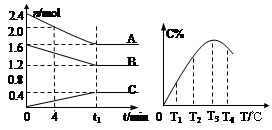
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2HI(g) 达到平衡状态时的标志是
2HI(g) 达到平衡状态时的标志是| A.混合气体的体积恒定不变 |
| B.混合气体的颜色不再改变 |
| C.H2、I2、HI的浓度相等 |
| D.I2在混合气体中的体积分数与H2在混合气体中的体积分数相等 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 xC(g)2min时反应达到平衡状态(温度不变),剩余了0.8molB,并测得C的浓度为0.4mol/L,请填写下列空白:
xC(g)2min时反应达到平衡状态(温度不变),剩余了0.8molB,并测得C的浓度为0.4mol/L,请填写下列空白:查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CO2(g)+H2(g);△H<0 试回答下列问题:
CO2(g)+H2(g);△H<0 试回答下列问题:查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 nW(g);ΔH,某化学兴趣小组的同学根据此反应在不同条件下的实验数据,作出了如下曲线图:
nW(g);ΔH,某化学兴趣小组的同学根据此反应在不同条件下的实验数据,作出了如下曲线图: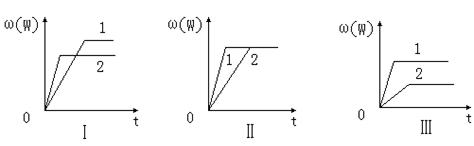
| A.图Ⅰ可能是不同压强对反应的影响,且p2>p1,a+b<n |
| B.图Ⅱ可能是不同压强对反应的影响,且p1>p2,n<a+b |
| C.图Ⅱ可能是在同温同压下催化剂对反应的影响,且1使用的催化剂效果好 |
| D.图Ⅲ可能是不同温度对反应的影响,且T1>T2,ΔH<0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com