
| A. | 硫酸铜的水溶液中,铜离子实际上主要以四水合铜离子的形式存在 | |
| B. | 氯化银沉淀能溶于氨水,说明有的配合物(或配离子)很稳定 | |
| C. | 金属离子都能作为中心离子,含有孤对电子的分子(或离子)都可作配体 | |
| D. | 硫氰合铁(III)离子呈血红色,由此可用KSCN溶液检验Fe3+离子 |
分析 A.硫酸铜的水溶液中,铜离子与水结合生成四水合铜离子;
B.氯化银沉淀能溶于氨水生成二氨合银离子;
C.配合物中,配位体提供孤电子对,中心原子提供空轨道形成配位键;
D.根据KSCN溶液与Fe3+离子反应生成硫氰合铁离子判断.
解答 解:A.硫酸铜的水溶液中,铜离子与水结合生成四水合铜离子,所以在水溶液中,铜离子实际上主要以四水合铜离子的形式存在,故A正确;
B.氯化银沉淀能溶于氨水生成二氨合银离子,说明有的配合物(或配离子)很稳定,故B正确;
C.配合物中,配位体提供孤电子对,中心原子提供空轨道形成配位键,而并不是所有金属离子都有空轨道,所以金属离子不是都能作为中心离子,故C错误;
D.KSCN溶液与Fe3+离子反应生成血红色的硫氰合铁离子,所以可用KSCN溶液检验Fe3+离子,故D正确;
故选C.
点评 本题考查了配合物的性质、配位键的形成等,难度不大,要明确形成配合物的条件是:有提供空轨道的中心原子,有提供孤电子对的配位体.


科目:高中化学 来源: 题型:选择题
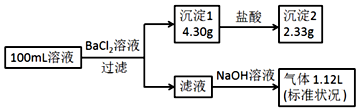
| A. | 原溶液一定存在CO32-和SO42-,一定不存在Fe3+ | |
| B. | 原溶液一定存在Cl-和Na+ | |
| C. | 原溶液中c(Cl-)≥0.2mol•L-1 | |
| D. | 若原溶液中c(NH4+)=0.05mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | A | B | C | D |
| 实验方案 |  |  |  |  |
| 实验目的 | 验证铁钉发生了析氢腐蚀 | 验证Fe电极被保护 | 验证乙烯的产生 | 验证甲烷与氯气发生了化学反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
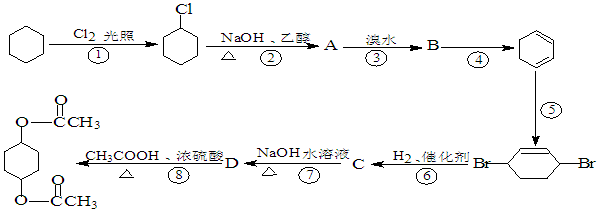
 ,C
,C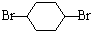 .
.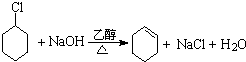 ; 反应⑦:
; 反应⑦: .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胆矾--FeSO4•7H2O | B. | 钡餐--BaCO3 | ||
| C. | 明矾--KAl(SO4)2 | D. | 生石膏--CaSO4•2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 反应Fe+H2SO4═FeSO4+H2↑的能量变化趋势如图所示:
反应Fe+H2SO4═FeSO4+H2↑的能量变化趋势如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 20.0 mL 18 mol•L-1 H2SO4溶液 | B. | 250.0 mL 2 mol•L-1 HCl溶液 | ||
| C. | 150.0 mL 2 mol•L-1 H2SO4溶液 | D. | 500.0 mL 3 mol•L-1 HCl溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com