
下列关于能源和作为能源物质的叙述中不正确的是( )
A.化学反应中的能量变化通常表现为热量的变化
B.天然气、石油、流水、风力为一次能源。
C.需要加热才能发生的反应一定是吸热反应
D.反应物总能量和生成物总能量的相对大小决定了反应是放出能量还是吸收能量
科目:高中化学 来源:2015-2016学年重庆市高二下第四次月考化学试卷(解析版) 题型:填空题
(1)2molO3和3molO2的质量之比为__________,同温同压下的密度之比为_________;
(2)向硅酸胶体中不断滴加稀氢氧化钠溶液的现象是_________;
(3)用质量分数为98%,密度为1.84g/cm3的浓硫酸配制100mL1.0mol•L-1稀硫酸操作中应用量筒量取_____mL浓硫酸,本实验用到的基本仪器已有烧杯、量筒、玻璃棒,还缺少的玻璃仪器是_________,配制过程中,下列情况会使配制结果偏低的是_________;①定容时俯视刻度线观察液面②未经冷却就进行转移操作③移液时未洗涤烧杯和玻璃棒④定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线。
(4)在标准状况下,由CO和CO2组成的混合气体6.72L,质量为12g,此混合物中CO和CO2的物质的量之比是_________,混合气体的平均相对分子质量是_________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年重庆一中高二下学期期中化学试卷(解析版) 题型:填空题
I.下列实验方案合理的是________。
A.在检验醛基配制银氨溶液时,在一定量氨水中,加入AgNO3溶液
B.在检验醛基配制Cu(OH)2悬浊液时,在一定量NaOH溶液中,滴加入少量CuSO4溶液
C.验证RX为碘代烃时,把RX与烧碱水溶液混合加热,将溶液冷却后直接加入硝酸银溶液
D.用电石与饱和食盐水反应时,将制得的气体先通入NaOH溶液,再通入酸性高锰酸钾溶液,可检验制得的气体是否为乙炔
E.乙烷中混有乙烯,通过氢气在一定条件下反应,使乙烯转化为乙烷
F.除去混在苯中的少量苯酚,加入过量溴水,过滤
G.实验室制取乙烯时必须将温度计的水银球插入反应液中,测定反应液的温度
II.现有通式为(CH2O)n的五种有机物,性质如下:
① 甲是无色有刺激性气味的气体,可以发生银镜反应;
② 乙、丙、丁的相对分子质量均为甲的2倍,戊的相对分子质量是甲的3倍;
③ 乙、戊的水溶液均可使紫色石蕊试液变红,还可以与乙醇在一定条件下酯化,且两分子戊可以形成六元环酯;
④ 丙既能水解,又能发生银镜反应;丁既能与钠反应放出H2,又能与新制Cu(OH)2悬浊液加热反应产生红色沉淀。
(1) 推断各物质的结构,写出其结构简式。
甲_________ ,乙_________ ,丙_________ ,丁_________ ,戊_________ 。
(2) 等物质的量的戊,分别与足量Na反应产生的气体和与足量NaHCO3反应产生的气体体积之比是______________( 在相同条件下测定)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州凯里一中高一下期中理科化学试卷(解析版) 题型:填空题
反应Fe+H2SO4===FeSO4+H2↑的能量变化趋势,如图所示:
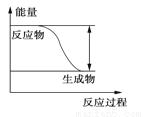
(1)该反应为________反应(填“吸热”或“放热”)。
(2)若要使该反应的反应速率加快,下列措施可行的是_____(填字母)。
A.改铁片为铁粉 B.增大压强
C.升高温度 D.改稀硫酸为98%的浓硫酸
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为______极(填“正”或“负”)。铜片上产生的现象为________________;该极上发生的电极反应为______________;外电路中电子由 _______极向_______极移动。(填“正”或“负”)
_______极向_______极移动。(填“正”或“负”)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州凯里一中高一下期中理科化学试卷(解析版) 题型:选择题
关于如图所示装置的叙述错误的是( )

A.锌是负极,其质量逐渐减小
B.氢离子在铜表面被还原
C.电子从锌片经导线流向铜片
D.电流从锌片经导线流向铜片
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州凯里一中高一下期中理科化学试卷(解析版) 题型:选择题
下列 关于物质性质变化的比较,不正确的是( )
关于物质性质变化的比较,不正确的是( )
A.酸性强弱:HIO4>HBrO4>HClO4 B.原子半径大小:Na>S>O
C.碱性强弱:KOH>NaOH>LiOH D.金属性强弱:Na>Mg>Al
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二5月月考理科化学试卷(解析版) 题型:填空题
(I) 某些石油中溶有一种碳氢化合物——金刚烷,它的分子立体结构如图所示:
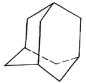
(1)由图可知其分子式为:____________;
(2)它是由4 个六元环构成的笼状结构,其中有___个碳原子为三个环共有;
(3)金刚烷分子的一氯代物有_______种。
(II)在烃的分子结构中,若每减少2个氢原子,则相当于碳碳间增加一对共用电子对。
(1)分子式为CnH2n-6的链状烃分子中碳碳间共用电子对数为 ___ __;
(2)Cx可看做是烃减氢后的产物,若某物质分子中碳碳间的共用电子对数为160,则符合该条件的碳单质的分子式为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二5月月考理科化学试卷(解析版) 题型:选择题
下列说法中,正确的是( )
A.同系物的物理性质相同
B.甲烷和环丙烷是同系物
C.相对分子质量相同的几种化合物互称为同分异构体
D.分子组成相差若干个CH2原子团的有机物不一定是同系物
查看答案和解析>>
科目:高中化学 来源:2015-2016学年青海师大附二中高一下期中化学试卷(解析版) 题型:填空题
(1)铅蓄电池是典型的可充型电池,电池总反应式为:Pb+PbO2+4H++2SO42-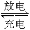 2PbSO4+2H2O。请回答下列问题(不考虑氢、氧的氧化还原):放电时,正极的电极反应式是____________;电解液中H2SO4的浓度将变________;当外电路通过1 mol电子时,理论上负极板的质量增加____g。
2PbSO4+2H2O。请回答下列问题(不考虑氢、氧的氧化还原):放电时,正极的电极反应式是____________;电解液中H2SO4的浓度将变________;当外电路通过1 mol电子时,理论上负极板的质量增加____g。
(2)微型纽扣电池在现代生活中有广泛应用。有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为Zn+2OH--2e-===ZnO+H2O,Ag2O+H2O+2e-===2Ag+2OH-。

根据上述反应式,完成下列题目。
(1)下列叙述正确的是________。
A.在使用过程中,电解质KOH被不断消耗
B.使用过程中,电子由Ag2O极经外电路流向Zn极
C.Zn是负极,Ag2O是正极
D.Zn电极发生还原反应,Ag2O电极发生氧化反应
(2)写出电池的总反应式:___________________________________________________________。
(3)使用时,负极区的pH________(填“增大”“减小”或“不变”,下同),正极区的pH______,电解质溶液的pH________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com