
在下列反应中画线物质做还原剂的是()。
A.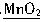 +4HCl=MnCl2+2H2O+Cl2↑
+4HCl=MnCl2+2H2O+Cl2↑
B.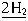 +O2=2H2O
+O2=2H2O
C.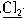 +2KI=2KCl+I2
+2KI=2KCl+I2
D.2Na+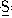 =Na2S
=Na2S
科目:高中化学 来源: 题型:阅读理解
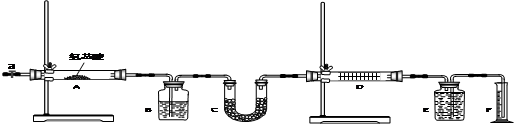
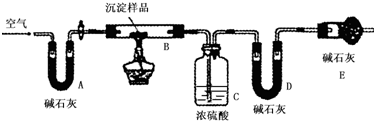
| B装置的质量(g) | C装置的质量(g) | D装置的质量(g) | |
| 实验前 | 15.4 | 262.1 | 223.8 |
| 试验后 | 6.1 | 264.8 | 230.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
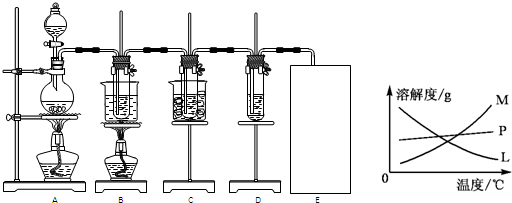
| ||
| ||
| ||
| 实验现象 | 原因 |
| 溶液最初从紫色逐渐变为 红 红 色 |
氯气与水反应生成的H+使石蕊变色 |
| 随后溶液逐渐变为无色 | 氯气与水反应生成的HClO将石蕊氧化为无色物质 氯气与水反应生成的HClO将石蕊氧化为无色物质 |
查看答案和解析>>
科目:高中化学 来源:2011届广东省惠能中学高三上学期第四次测试理综化学部分 题型:填空题
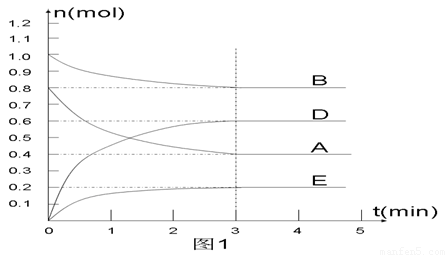
在某个容积为2 L的密闭容器内,在T1℃时按下图1所示发生反应:
mA(g)+nB(g)  pD(g)+qE(s),DH<0(m、n、p、q为最简比例的整数)。
pD(g)+qE(s),DH<0(m、n、p、q为最简比例的整数)。 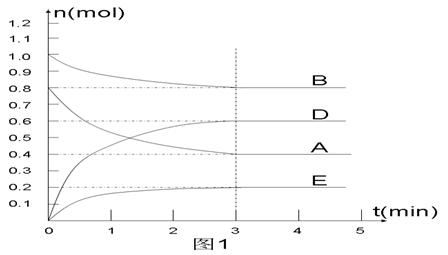
(1)据图1所示,反应开始至达到平衡时,用D表示该反应速率为_____________;
(2)该反应的化学平衡常数K的表达式为________________________________;
(3) 下列措施能增大B的转化率的是 ( )
| A.升高温度 |
| B.保持体积不变通入1molB |
| C.保持体积不变移出部分物质D(g) |
| D.将容器的容积增大为原来2倍 |
查看答案和解析>>
科目:高中化学 来源:2010-2011学年广东省高三上学期第四次测试理综化学部分 题型:填空题
在某个容积为2 L的密闭容器内,在T1℃时按下图1所示发生反应:
mA(g)+nB(g)  pD(g)+qE(s),DH<0(m、n、p、q为最简比例的整数)。
pD(g)+qE(s),DH<0(m、n、p、q为最简比例的整数)。
(1)据图1所示,反应开始至达到平衡时,用D表示该反应速率为_____________;
(2)该反应的化学平衡常数K的表达式为________________________________;
(3) 下列措施能增大B的转化率的是 ( )
A.升高温度
B.保持体积不变通入1molB
C.保持体积不变移出部分物质D(g)
D.将容器的容积增大为原来2倍
E. 保持体积不变通入1mol A
(4) 反应开始时向容器中通入一定量的A和B,反应达到平衡时,测得D的浓度为0.6 mol.L-1 。(图2中纵坐标为D的浓度)
①请用实线在下图坐标系中该表示平衡的建立过程。
②若该反应在T2℃(T2> T1)温度下进行,请用虚线画出该平衡的建立过程。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com