
氨气是化学工业上应用非常广泛的物质。下面仅是它在两方面的重要用途。
“侯氏制碱法”的发明为振兴中国化工工业做出了重要贡献。制碱法的第一步反应是向饱和氨化盐水中通入二氧化碳,该反应可表示为:NaCl + CO2 + NH3 + H2O → NaHCO3↓+ NH4Cl
现在45℃时,取117g食盐配制成饱和溶液,向其中通入适量氨气后,再向其中通入二氧化碳,使反应进行完全。试计算并回答下列问题(计算结果取三位有效数字)(有关物质的溶解度数据如表,单位:g/100g水)。
|
|
NaCl |
NaHCO3 |
NH4Cl |
|
10℃ |
35.8 |
8.15 |
33.0 |
|
45℃ |
37.0 |
14.0 |
50.0 |
(1)117g食盐理论上可以制取纯碱 g;
(2)45℃反应完毕后,有晶体析出;溶液中剩余水 g,析出晶体的质量 g。
(3)过滤除去析出的晶体后再降温至10℃,又有晶体析出,计算所析出晶体的质量共 克
工业制硝酸也是氨气重要用途之一,反应如下:
4NH3+5O2→4NO+6H2O 2NO+O2→2NO2 3NO2+H2O→2HNO3+NO
将a mol的NH3与b mol的O2混合后,充入一密闭容器,在Pt存在下升温至700℃,充分反应后,冷却至室温。
 (4)请讨论b∕a的取值范围及与之对应的溶液的溶质及其物质的量,将结果填于下表中:
(4)请讨论b∕a的取值范围及与之对应的溶液的溶质及其物质的量,将结果填于下表中:
|
b∕a的取值范围 |
溶质 |
溶质物质的量 |
|
|
|
|
|
|
—— |
—— |
|
|
|
|
|
|
|
|
(1)106g (1分)
(2)280 g 129g (2分)
(3)共30.9g(3分)(其中NH4Cl 14.5g,NaHCO316.4g)
(4)(共6分)
|
b∕a的取值范围 |
溶质 |
溶质物质的量 |
|
0<b∕a<5∕4 (0.5分) |
NH3 (0.5分) |
(a-4b∕5)mol (1分) |
|
b∕a=5∕4 |
/ |
/ |
|
5∕4<b∕a<2 (0.5分) |
HNO3 (0.5分) |
(4b-5a) ∕3mol (1分) |
|
b∕a≥2 (0.5分) |
HNO3 (0.5分) |
amol (1分) |
【解析】
试题分析:
(1)根据计量数可求得得106g。
(2)在45℃时,取117g食盐配制成饱和溶液,需水xg,117/x=37.0/100解得x=316.0,反应消耗水2mol(36g),剩余水280g;其中容纳NaHCO3为39g析出晶体NaHCO3为129g。
(3)根据溶解度计算共30.9g(其中NH4Cl 14.5g,NaHCO316.4g)。
(4)若0<b∕a<5∕4 ,氨气反应不完,剩余氨气;5∕4<b∕a<2,氨气完全转变为NO,但NO只能部分反应生成HNO3,得HNO3为 (4b-5a) ∕3mol ;N完全转化为硝酸为amol。
53.跟据题意主链为OHC-C-C-CHO,另外两个-CH3和一个Br共有5种连接方式。
考点:本题考查了溶解度、化学反应计算等基本知识。


 名师点拨卷系列答案
名师点拨卷系列答案科目:高中化学 来源: 题型:阅读理解
| NaCl | NaHCO3 | NH4Cl | |
| 10℃ | 35.8 | 8.15 | 33.0 |
| 45℃ | 37.0 | 14.0 | 50.0 |
| b∕a的取值范围 | 溶质 | 溶质物质的量 | ||||
0<b∕a<5∕4 0<b∕a<5∕4 |
NH3 NH3 |
(a-4b∕5)mol (a-4b∕5)mol | ||||
|
-- | -- | ||||
5∕4<b∕a<2 5∕4<b∕a<2 |
HNO3 HNO3 |
(4b-5a)∕3mol (4b-5a)∕3mol | ||||
b∕a≥2 b∕a≥2 |
HNO3 HNO3 |
amol amol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| NaCl | NaHCO3 | NH4Cl | |
| 10℃ | 35.8 | 8.15 | 33.0 |
| 45℃ | 37.0 | 14.0 | 50.0 |
| b∕a的取值范围 | 溶质 | 溶质物质的量 |
| ______ | ______ | ______ |
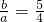 | -- | -- |
| ______ | ______ | ______ |
| ______ | ______ | ______ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com