
| 反应 过程 | 化学方程式 | 焓变△H (kJ/mol) | 正反应活化能Ea (kJ/mol) |
| 甲烷 氧化 | CH4(g)+2O2(g)=CO2(g)+2H2O(g) | -802.6 | 125.6 |
| CH4(g)+O2(g)=CO2(g)+2H2(g) | -322.0 | 172.5 | |
| 蒸汽 重整 | CH4(g)+H2O(g)=CO(g)+3H2(g) | 206.2 | 240.1 |
| CH4(g)+2H2O(g)=CO2(g)+4H2(g) | 165.0 | 243.9 |
分析 (1)根据盖斯定律,由蒸汽重整的两个反应CH4(g)+2H2O(g)=CO2(g)+4H2(g)减CH4(g)+H2O(g)=CO(g)+3H2(g),可得反应:CO(g)+H2O(g)=CO2(g)+H2(g),据此计算反应热;
(2)由表中数据可知,甲烷氧化的活化能低于蒸气重整的活化能,活化能越低,反应速率越快;
(3)根据平衡常数k的表达式,利用信息直接书写Kp;
该反应为吸热反应,升高温度,平衡向正反应移动,平衡常数增大;
(4)从能量的角度分析,放热的甲烷氧化反应为吸热的蒸气重整提供能量;
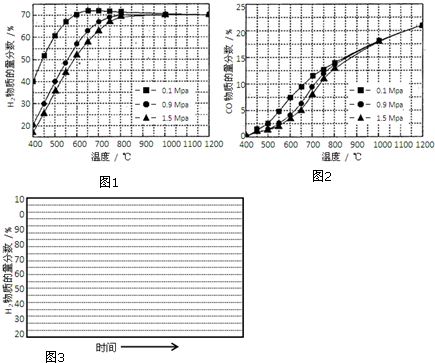
(5)①根据图象中,温度、压强对H2和CO物质的量分数的影响数据,选择判断;
②结合图象可知在600℃、0.1 MPa的条件下,平衡时系统中H2的物质的量分数达到70%,起始进料时H2的物质的量分数为0,据此可画出H2的物质的量分数随时间变化的示意图;
(6)如果反应过程中进氧气的量过大,会导致生成的氢气和氧气反应,导致质量分数降低.
解答 解:(1)根据盖斯定律,由蒸汽重整的两个反应CH4(g)+2H2O(g)=CO2(g)+4H2(g)减CH4(g)+H2O(g)=CO(g)+3H2(g),可得反应:CO(g)+H2O(g)=CO2(g)+H2(g),故△H=165.0kJ/mol-206.2kJ/mol=-41.2kJ/mol,
故答案为:-41.2;
(2)由表中数据可知,甲烷氧化的活化能低于蒸气重整的活化能,活化能越低,反应速率越快,故初始阶段,甲烷蒸汽重整的反应速率小于甲烷氧化的反应速率,
故答案为:小于;
(3)根据平衡常数k的表达式,可知反应CH4(g)+H2O(g)?CO(g)+3H2(g)的KP=$\frac{{p}^{3}({H}_{2})p(CO)}{p(C{H}_{4})p({H}_{2}O)}$,
该反应为吸热反应,升高温度,平衡向正反应移动,平衡常数增大,
故答案为:$\frac{{p}^{3}({H}_{2})p(CO)}{p(C{H}_{4})p({H}_{2}O)}$;增大;
(4)从能量的角度分析,甲烷自热重整方法的先进之处在于:放热的甲烷氧化反应为吸热的蒸气重整提供能量,提高能源的利用率,
故答案为:系统内强放热的甲烷氧化反应为强吸热的蒸汽重整反应提供了所需的能量;
(5)①由图中数据可知,0.9 MPa时,H2的物质的量分数>65%,CO物质的量分数<10%,则700℃符合,1.5 MPa时,H2的物质的量分数>65%,CO物质的量分数<10%,则温度要高于750℃,低于约725℃,矛盾,故B正确,ACD错误,故答案为:B;
②起始进料时H2的物质的量分数为0,结合图象可知600℃,0.1 MPa的条件下,平衡时系统中H2的物质的量分数达到70%,据此画出H2的物质的量分数随时间变化的示意图为 ,故答案为:
,故答案为: ;
;
(6)如果反应过程中进氧气的量过大,会导致生成的氢气和氧气反应,导致质量分数降低,故答案为:甲烷氧化程度过高,导致生成的氢气和氧气反应.
点评 本题考查热化学以及化学反应速率、化学平衡等,意在考查考生分析、处理数据和解答图象试题的能力,解答本题需利用盖斯定律,联系化学平衡、化学平衡常数以及平衡移动原理等,弄清图象的含义,题目难度中等.


 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:推断题
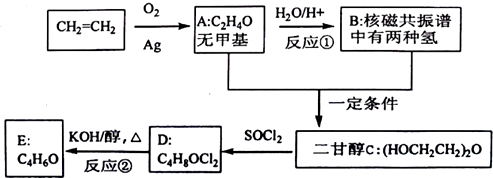
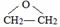 、DClCH2CH2OCH2CH2Cl.
、DClCH2CH2OCH2CH2Cl.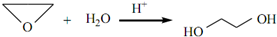 ;反应②ClCH2CH2OCH2CH2Cl+2KOH$→_{△}^{乙醇}$CH2=CH-O-CH=CH2+2KCl+2H2O.
;反应②ClCH2CH2OCH2CH2Cl+2KOH$→_{△}^{乙醇}$CH2=CH-O-CH=CH2+2KCl+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单位时间内生成nmolA2,同时消耗2n molAB | |
| B. | AB的消耗速率等于A2的消耗速率 | |
| C. | 容器内,3种气体AB、A2、B2共存 | |
| D. | 容器中各组分的体积分数不随时间变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Zn 粒与稀硫酸反应制取氢气 | |
| B. | 二氧化碳与氢氧化钠溶液反应生成碳酸钠 | |
| C. | 氧化铁在高温下与一氧化碳反应 | |
| D. | 碳酸钠溶液与石灰乳混合 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 重金属、农药等会造成水体污染 | |
| B. | 装饰材料中的甲醛、苯等会造成居室污染 | |
| C. | CO会导致酸雨的形成 | |
| D. | CO2的大量排放会加剧温室效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
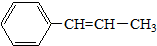 )的叙述正确的是( )
)的叙述正确的是( )| A. | 最多有5个碳原子在一条直线上 | |
| B. | 发生加聚反应的产物为: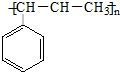 | |
| C. | 所有碳原子可能在同一平面上 | |
| D. | 1 mol该物质最多能与3 mol H2发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,3.2g O2和3.2g O3所含氧原子数都是0.2NA | |
| B. | 常温下,0.1mol•L-1NH4NO3溶液中,含有的氮原子数是0.2NA | |
| C. | 0.1molN2与足量的H2反应,转移的电子数是0.6NA | |
| D. | 2.24LCO和CO2的混合气体中所含的碳原子数一定是NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com