
¹¤ŅµÉś²śĮņĖįŹ±£¬ĘäÖŠŅ»²½·“Ó¦ŹĒ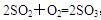 £¬ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ(””””)
£¬ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ(””””)
A”¢Ōö“óŃõĘųµÄÅضČæÉĢįøß·“Ó¦ĖŁĀŹ
B”¢ÉżøßĪĀ¶ČæÉĢįøß·“Ó¦ĖŁĀŹ
C”¢Ź¹ÓĆ“ß»Æ¼ĮÄÜĻŌÖųŌö“ó·“Ó¦ĖŁĀŹ
D”¢“ļµ½»ÆŃ§Ę½ŗāŹ±ÕżÄę·“Ó¦ĖŁĀŹĻąµČĒŅ¶¼ĪŖĮć
 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
½«Na2O2Öš½„¼ÓČėµ½ŗ¬ÓŠAl3£«”¢Mg2£«”¢NH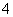 µÄ»ģŗĻŅŗÖŠ²¢Ī¢ČČ£¬²śÉś³ĮµķŗĶĘųĢåµÄĪļÖŹµÄĮæÓė¼ÓČėNa2O2µÄĪļÖŹµÄĮæµÄ¹ŲĻµČēĻĀĶ¼ĖłŹ¾£¬ŌņŌ»ģŗĻŅŗÖŠAl3£«”¢Mg2£«”¢NH
µÄ»ģŗĻŅŗÖŠ²¢Ī¢ČČ£¬²śÉś³ĮµķŗĶĘųĢåµÄĪļÖŹµÄĮæÓė¼ÓČėNa2O2µÄĪļÖŹµÄĮæµÄ¹ŲĻµČēĻĀĶ¼ĖłŹ¾£¬ŌņŌ»ģŗĻŅŗÖŠAl3£«”¢Mg2£«”¢NH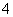
 µÄĪļÖŹµÄĮæ·Ö±šŹĒ
µÄĪļÖŹµÄĮæ·Ö±šŹĒ
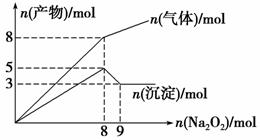
A£®2 mol”¢3 mol”¢4 mol”””””” B£®2 mol”¢3 mol”¢8 mol
C£®3 mol”¢2 mol”¢8 mol D£®3 mol”¢2 mol”¢4 mol
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ČēĶ¼ĖłŹ¾£¬Éձ֊װӊĻ”ĮņĖį£¬A”¢B”¢C”¢D·Ö±šĪŖĶ”¢Šæ”¢Ģ¼°ō”¢Ģ¼°ō£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ(””””)
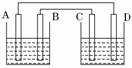
A£®A”¢D°ōÉĻ¾ł²śÉśĘųÅŻ
B£®B”¢C°ōÉĻ¾ł²śÉśĘųÅŻ
C£®µē×ÓĮ÷¶Æ·½ĻņA”śD
D£®×ó±ßÉÕ±ÖŠČÜŅŗµÄpH»į½µµĶ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŅŌĻĀ¹ŲÓŚ»Æѧ·“Ó¦ĖŁĀŹµÄĖµ·ØÕżČ·µÄŹĒ(””””)
A”¢»Æѧ·“Ó¦ĖŁĀŹæÉÓĆijŹ±æĢÉś³ÉĪļµÄÖŹĮæŌö¼ÓĄ“±ķŹ¾
B”¢ŌŚĶ¬Ņ»·“Ó¦ÖŠ£¬ÓĆø÷ÖÖĪļÖŹ±ķŹ¾µÄ»Æѧ·“Ó¦ĖŁĀŹµÄ“óŠ”ĻąµČ
C”¢»Æѧ·“Ó¦ĖŁĀŹÖøµ„Ī»Ź±¼äÄŚ·“Ó¦ĪļÅØ¶ČµÄ¼õÉŁ»ņÉś³ÉĪļÅØ¶ČµÄŌö¼Ó
D”¢Čō·“Ó¦ĻÖĻóŌŚ¶ĢŹ±¼äÄŚ³öĻÖ£¬Ōņ·“Ó¦ĖŁĀŹæģ£¬ČōĪŽĆ÷ĻŌĻÖĻó£¬Ōņ·“Ó¦ĖŁĀŹĀż
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŌŚĆܱÕČŻĘ÷ÖŠ£¬NO(g)£«CO(g) 
 N2(g)£«CO2(g)¦¤H£½£373.2 kJ”¤mol£1”£“ļµ½Ę½ŗāŗó£¬ĪŖĮĖĢįøßøĆ·“Ó¦µÄĖŁĀŹŗĶNOµÄ×Ŗ»ÆĀŹ£¬²ÉČ”µÄ“ėŹ©ÕżČ·µÄŹĒ(””””)
N2(g)£«CO2(g)¦¤H£½£373.2 kJ”¤mol£1”£“ļµ½Ę½ŗāŗó£¬ĪŖĮĖĢįøßøĆ·“Ó¦µÄĖŁĀŹŗĶNOµÄ×Ŗ»ÆĀŹ£¬²ÉČ”µÄ“ėŹ©ÕżČ·µÄŹĒ(””””)
A”¢¼Ó“߻ƼĮ£¬Ķ¬Ź±ÉżøßĪĀ¶Č
B”¢¼Ó“߻ƼĮ£¬Ķ¬Ź±Ōö“óŃ¹Ēæ
C”¢ÉżøßĪĀ¶Č£¬Ķ¬Ź±³äČėN2
D”¢½µµĶĪĀ¶Č£¬Ķ¬Ź±Ōö“óŃ¹Ēæ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĮņĖįŹĒŅ»ÖÖÖŲŅŖµÄ»Æ¹¤²śĘ·£¬ĮņĖįµÄĻūŗÄĮæ³£±»ŹÓĪŖŅ»øö¹ś¼Ņ¹¤Ņµ·¢“ļĖ®Ę½µÄŅ»ÖÖ±źÖ¾”£ÄæĒ°µÄÖŲŅŖÉś²ś·½·ØŹĒ”°½Ó“„·Ø”±£¬ÓŠ¹Ų½Ó“„Ńõ»Æ·“Ó¦2SO2£«O2“߻ƼĮ2SO3µÄĖµ·Ø²»ÕżČ·µÄŹĒ(””””)
A”¢øĆ·“Ó¦ĪŖæÉÄę·“Ó¦£¬¹ŹŌŚŅ»¶ØĢõ¼žĻĀ¶žŃõ»ÆĮņŗĶŃõĘų²»æÉÄÜČ«²æ×Ŗ»ÆĪŖČżŃõ»ÆĮņ
B”¢“ļµ½Ę½ŗāŗ󣬷“Ó¦¾ĶĶ£Ö¹ĮĖ£¬¹ŹÕż”¢Äę·“Ó¦ĖŁĀŹĻąµČĒŅ¾łĪŖĮć
C”¢Ņ»¶ØĢõ¼žĻĀ£¬ĻņijĆܱÕČŻĘ÷ÖŠ¼ÓČė2molSO2ŗĶ1molO2£¬Ōņ“Ó·“Ó¦æŖŹ¼µ½“ļµ½Ę½ŗāµÄ¹ż³ĢÖŠ£¬Õż·“Ó¦ĖŁĀŹ²»¶Ļ¼õŠ”£¬Äę·“Ó¦ĖŁĀŹ²»¶ĻŌö“ó£¬Ä³Ņ»Ź±æĢ£¬Õż”¢Äę·“Ó¦ĖŁĀŹĻąµČ
D”¢ŌŚĄūÓĆÉĻŹö·“Ӧɜ²śČżŃõ»ÆĮņŹ±£¬ŅŖĶ¬Ź±æ¼ĀĒ·“Ó¦ĖłÄÜ“ļµ½µÄĻŽ¶ČŗĶ»Æѧ·“Ó¦ĖŁĀŹĮ½·½ĆęµÄĪŹĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
³żČ„FeSO4ČÜŅŗÖŠÉŁĮæµÄĮņĖįĢś£¬æÉŠŠµÄ°ģ·ØŹĒ
A£®¼ÓČėĢś·Ū B£®¼ÓČėĶ·Ū
C£®¼ÓČėĒāŃõ»ÆÄĘČÜŅŗ D£®µĪČėKSCNČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠÓŠ¹ŲĪļÖŹÓ¦ÓƵÄĖµ·ØÕżČ·µÄŹĒ
A£®ÉśŹÆ»ŅÓĆ×÷Ź³Ę·æ¹Ńõ¼Į B£®ŃĪĄą¶¼æÉ×÷µ÷Ī¶Ę·
C£®ĀĮ¹ŽæÉ¾ĆŹ¢Ź³“× D£®Š”ĖÕ“ņŹĒĆę°ü·¢½Ķ·ŪµÄÖ÷ŅŖ³É·Ö
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŅŃÖŖ·“Ó¦£ŗ¢Ł101 kPaŹ±£¬2C(s)+O2(g)====2CO(g) ¦¤H=-221 kJ”¤mol-1
¢ŚĻ”ČÜŅŗÖŠ£¬H+(aq)+OH-(aq) ====H2O(l) ¦¤H=-57.3 kJ”¤mol-1
ĻĀĮŠ½įĀŪÕżČ·µÄŹĒ( )
A.Ģ¼µÄČ¼ÉÕČČ“óÓŚ110.5 kJ”¤mol-1
B.¢ŁµÄ·“Ó¦ČČĪŖ221 kJ”¤mol-1
C.Ļ”ĮņĖįÓėĻ”NaOHČÜŅŗ·“Ó¦µÄÖŠŗĶČČĪŖ-57.3 kJ”¤mol-1
D.Ļ”“×ĖįÓėĻ”NaOHČÜŅŗ·“Ӧɜ³É1 molĖ®£¬·Å³ö57.3 kJČČĮæ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com