
 某同学设计如图装置,研究非金属元素性质变化规律.
某同学设计如图装置,研究非金属元素性质变化规律.分析 (1)中装浓盐酸,B中装高锰酸钾溶液反应生成氯气具有氧化性,通入饱和氢硫酸溶液,反应开始后观察现象是C中产生淡黄色沉淀,说明氯气氧化硫化氢为硫单质;单质氧化剂的氧化性大于氧化产物,判断非金属性;
(2)氯气将碘离子氧化为碘单质,碘单质遇到淀粉变蓝色;
(3)有机强酸能制弱酸的规律结合硝酸溶液、碳酸钙、澄清石灰水、硅酸钠溶液,选择试剂用如图装置证明:酸性:HNO3>H2CO3>H2SiO3可以得到:非金属性:N>C>Si.
解答 解:(1)果C中装饱和氢硫酸溶液,A中装浓盐酸,B中装高锰酸钾溶液,反应开始后观察现象是C中产生淡黄色沉淀,反应的化学方程式为:Cl2+H2S═S↓+2HCl;证明氯元素比硫元素非金属性强,故答案为:强;
(2)盐酸和高锰酸钾之间反应产生氯气,氯气将碘离子氧化为碘单质,碘单质遇到淀粉变蓝色,故答案为:淀粉-KI溶液变蓝色;
(3)现有硝酸溶液、碳酸钙、澄清石灰水、硅酸钠溶液,选择试剂用如图装置证明:酸性:HNO3>H2CO3>H2SiO3;因此先加入硝酸和碳酸钙反应生成二氧化碳,二氧化碳通入硅酸钠溶液生成硅酸沉淀;装置C中反应是:CO2+SiO32-+H2O=H2SiO3↓+CO32-,C中装试剂硅酸钠溶液;现象为有白色沉淀生成;但是浓硝酸具有挥发性,防止硝酸和硅酸钠之间反应的干扰,所以在B、C之间加一个盛饱和NaHCO3溶液的洗气瓶,
故答案为:硅酸钠溶液;有白色沉淀生成;在B、C之间加一个盛饱和NaHCO3溶液的洗气瓶.
点评 本题考查了酸性强弱的比较实验设计,试剂选择,离子方程式的书写,熟练掌握物质性质是解题关键.题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
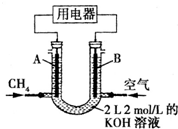 将CH4设计成燃料电池,其利用率更高,装置如右图所示(A、B为多孔碳棒).持续通入甲烷,在标准状况下,消耗甲烷的体积为V L.
将CH4设计成燃料电池,其利用率更高,装置如右图所示(A、B为多孔碳棒).持续通入甲烷,在标准状况下,消耗甲烷的体积为V L.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硝基苯中混有的少量硫酸和硝酸,将其倒入盛有NaOH溶液的分液漏斗中,振荡,静置,分液 | |
| B. | 乙烷中混有乙烯,通入氢气在一定条件下反应,使乙烯转化为乙烷 | |
| C. | 溴苯中混有溴,加入KI溶液,振荡,用汽油萃取出碘 | |
| D. | 乙烯中混有SO2和CO2,将其通入溴水中洗气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增加CO的量 | B. | 增大压强 | C. | 升高温度 | D. | 加入稀有气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ⑤⑦ | B. | ②④⑥⑧ | C. | ③④ | D. | ①③⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 高铁酸钾(K2FeO4)具有极强的氧化性,可作为水处理剂和高容量电池材料.
高铁酸钾(K2FeO4)具有极强的氧化性,可作为水处理剂和高容量电池材料.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油裂解可获得乙烯、丙烯和丁二烯 | |
| B. | 煤干馏可以得到甲烷、苯和氨等重要化工原料 | |
| C. | 天然植物油常温下一般呈液态,难溶于水,有固定的熔点、沸点 | |
| D. | 酚醛树脂、聚酯纤维(涤纶)都是由缩聚反应制得的高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 时间/s | 0 | 20 | 40 | 60 | 80 | 100 |
| c(NO2)/mol•L-1 | 0.00 | 0.12 | 0.20 | 0.26 | 0.30 | 0.30 |
| A. | 升高温度该反应的平衡常数K减小 | |
| B. | 该反应的△S<0 | |
| C. | 反应达平衡时吸热15.9kJ | |
| D. | 100s 时再通入0.40 mol N2O4,达新平衡时N2O4的转化率减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com