
| A、CH2Cl2 |
| B、CH3CH2Cl |
| C、CH3CH2OH |
| D、CH2ClCH2Cl |


 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源: 题型:
| A、3mol?L-1 |
| B、2mol?L-1 |
| C、1.5mol?L-1 |
| D、1mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液中含有1 mol NaCl |
| B、1 L溶液里含有NaCl 58.5克 |
| C、58.5 g NaCl溶于941.5 g水中 |
| D、1 mol NaCl溶于1 L水中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、制取蒸馏水时,为防止烧瓶内产生暴沸现象,应先向烧瓶中加入几片碎瓷片 |
| B、在用系列实验装置制取和检验的实验中,尾气污染空气,一定要用水吸收尾气 |
| C、用加热KMnO4的方法制得的氧气中常带有紫色,应在靠近试管口处放一团棉花 |
| D、在点燃甲烷气体前,为防止爆炸,应先验纯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
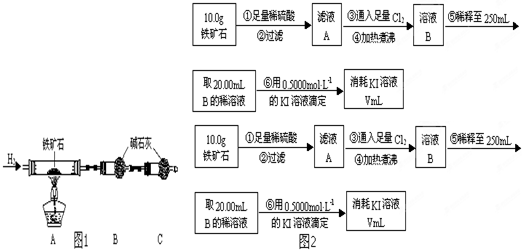
查看答案和解析>>
科目:高中化学 来源: 题型:
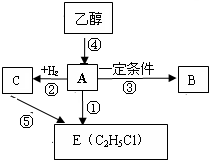 气态有机物 A在标准状况下密度为1.25g/L,A在一定条件下可以合成聚合物B,B可作食品包装袋.
气态有机物 A在标准状况下密度为1.25g/L,A在一定条件下可以合成聚合物B,B可作食品包装袋.查看答案和解析>>
科目:高中化学 来源: 题型:
 2SO2(g)+O2(g)=2SO3(G)反应过程的能量变化如图所示.已知l mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ?mol-1.请回答下问题;
2SO2(g)+O2(g)=2SO3(G)反应过程的能量变化如图所示.已知l mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ?mol-1.请回答下问题;| 1 |
| 3 |
| 1 |
| 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)铝热反应原理
(1)铝热反应原理| 实验步骤 | 现象 | 结论 |
| ①取少量黑色固体于试管中加稀盐酸 | 固体全部溶解,有气泡产生 | 假设Ⅰ成立,假设Ⅱ不成立 |
| ②滴入几滴0.01mo1/L KSCN溶液 | 深液不变色 |
| 编号 | 实验步骤 |
| 1 | ①滴加饱和FeC13溶液4滴,充分振荡 |
| ②滴加几滴NaOH溶液 | |
| 2 | ①滴加4滴1mol?L-1 KSCN溶液 |
| ②滴加几滴NaOH溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com