
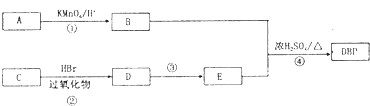
 ���ܼ���һ�����Ӳ��ϵ������Ի�ʹ����Һ�������Ӽ�����������ʳƷ���������ҵ��DBP�����ܼ���һ�֣�����ʽΪC16H22O4�����ɳ����Ĺ�ҵԭ��A������ʽΪC8H10����C�ϳ�DBP��·����ͼ��ʾ��
���ܼ���һ�����Ӳ��ϵ������Ի�ʹ����Һ�������Ӽ�����������ʳƷ���������ҵ��DBP�����ܼ���һ�֣�����ʽΪC16H22O4�����ɳ����Ĺ�ҵԭ��A������ʽΪC8H10����C�ϳ�DBP��·����ͼ��ʾ��| 0.448L |
| 22.4L/mol |
| 1.66 |
| 0.02 |
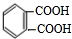 ��AΪ
��AΪ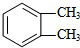 ��B��E��Ӧ�õ�DBPӦ�Ƿ���������Ӧ����E�����������ܹ�����������Ӧ����E���д��ǻ������ǻ�������Cԭ���Ϻ���2��Hԭ�ӣ�DBP�ķ���ʽΪC16H22O4���䲻���Ͷ�Ϊ
��B��E��Ӧ�õ�DBPӦ�Ƿ���������Ӧ����E�����������ܹ�����������Ӧ����E���д��ǻ������ǻ�������Cԭ���Ϻ���2��Hԭ�ӣ�DBP�ķ���ʽΪC16H22O4���䲻���Ͷ�Ϊ| 2��16+2-22 |
| 2 |
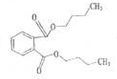 ���ݴ˽��
���ݴ˽��| 0.448L |
| 22.4L/mol |
| 1.66 |
| 0.02 |
 ��AΪ
��AΪ ��B��E��Ӧ�õ�DBPӦ�Ƿ���������Ӧ����E�����������ܹ�����������Ӧ����E���д��ǻ������ǻ�������Cԭ���Ϻ���2��Hԭ�ӣ�DBP�ķ���ʽΪC16H22O4���䲻���Ͷ�Ϊ
��B��E��Ӧ�õ�DBPӦ�Ƿ���������Ӧ����E�����������ܹ�����������Ӧ����E���д��ǻ������ǻ�������Cԭ���Ϻ���2��Hԭ�ӣ�DBP�ķ���ʽΪC16H22O4���䲻���Ͷ�Ϊ| 2��16+2-22 |
| 2 |
 ��
�� ��EΪCH3CH2CH2CH2OH�����еĹ��������ǻ����ʴ�Ϊ��
��EΪCH3CH2CH2CH2OH�����еĹ��������ǻ����ʴ�Ϊ�� �ǻ���
�ǻ��� ������Ϊ�ڱ������ᣬ�ʴ�Ϊ���ڱ������
������Ϊ�ڱ������ᣬ�ʴ�Ϊ���ڱ������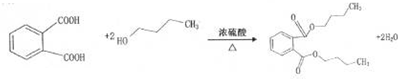 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��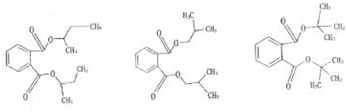 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
�� �����ܻ����к�������������������֬��Ͱװ�����������Ϻ�װֲ�������������϶��ܻ������ʴ�Ϊ��bc��
�����ܻ����к�������������������֬��Ͱװ�����������Ϻ�װֲ�������������϶��ܻ������ʴ�Ϊ��bc��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
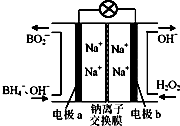 �ݱ����������⻯����NaBH4��BԪ�صĻ��ϼ�Ϊ+3�ۣ���H2O2��ԭ�ϵ�ȼ�ϵ�أ��������ϲ���Pt/C���������ϲ���MnO2���������վ�ͨ�����ǵ�Դ���乤��ԭ����ͼ��ʾ������˵����ȷ���ǣ�������
�ݱ����������⻯����NaBH4��BԪ�صĻ��ϼ�Ϊ+3�ۣ���H2O2��ԭ�ϵ�ȼ�ϵ�أ��������ϲ���Pt/C���������ϲ���MnO2���������վ�ͨ�����ǵ�Դ���乤��ԭ����ͼ��ʾ������˵����ȷ���ǣ�������| A����طŵ�ʱNa+��b��������a���� |
| B��ÿ����3 mol H2O2��ת�Ƶĵ���Ϊ3 mol |
| C���缫a����MnO2��MnO2�����缫�������д����� |
| D���õ�صĸ�����ӦʽΪ��BH4-+8OH--8e-=BO2-+6H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��
| ||
B��
| ||
C��
| ||
D��
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����״���£�22.4LH2O����NA������ |
| B��1L1mol?L -1��NaClO ��Һ�к���ClO-����Ŀ����NA�� |
| C��0.1molAlCl3��ȫת��Ϊ�����������壬����0��lNA���������� |
| D��0.1molCl2������NaOH��Һ��Ӧ��ת�Ƶ�����Ϊ0.2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������£�17.6g�����������ļ��Թ��ۼ�Ϊ4NA |
| B�������£�21.0g��ϩ�Ͷ�ϩ�Ļ�������к��е�̼ԭ����ĿΪ1.5NA |
| C�������£���5.6g��Ͷ�뵽����Ũ�����У���Ӧת�Ƶĵ�����ĿΪ0.3NA |
| D��12 g���ʯ�к��еĹ��ۼ���Ϊ4 NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Ba��OH��2��Һ�еμ�NaHSO4��Һ�����ԣ�Ba2++OH-+H++SO42-=BaSO4��+H2O |
| B�����Ȼ�����Һ��������ˮ��Ӧ��Al3++4NH3?H2O=AlO2-+4NH4++2H2O |
| C����1mol KAl��SO4��2����Һ�����Ba��OH��2�����ɳ������������ʱ�����ӷ���ʽ��2Al3++3SO42-+3Ba2++6OH-=2 Al��OH��3��+3BaSO4�� |
| D�������ʯ��ˮ�м��뼸��NaHCO3��Һ��Ca2++OH-+HCO3-=CaCO3��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
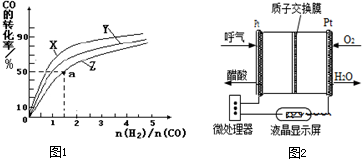
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com