
| A. | 钝化 | B. | 焰色反应 | C. | 风化 | D. | 电解质溶液导电 |
分析 有新物质生成的变化是化学变化,没有新物质生成的变化是物理变化,不需要化学变化就表现出来的性质是物理性质,如颜色、状态、气味、熔沸点、密度、硬度、溶解性等,需要发生化学反应才能表现出来的性质是化学性质,如:酸性、碱性、氧化性、还原性、热稳定性等,据此分析解答.
解答 解:A.铝、铁和浓硫酸或浓硝酸发生氧化还原反应生成一层致密的氧化物薄膜而阻止进一步被氧化,有新物质生成,属于化学变化,故A错误;
B.焰色反应是某些金属或它们的化合物在无色火焰中灼烧时使火焰呈现特征颜色的反应,没有新物质生成,属于物理变化,故B正确;
C.风化是结晶水化物在室温和干燥空气里失去结晶水的现象,有新物质生成,属于化学变化,故C错误;
D.电解质溶液的导电:离子在外加电场的作用下发生定向移动,无新物质生成,属于物理变化,但在电极附近,有氧化还原反应发生,阳极附近,阴离子失去电子被氧化;阴极附近,阳离子得电子被还原,属于化学变化,故D错误;
故选B.
点评 本题考查化学变化和物理变化判断,侧重考查基本概念,物理变化与化学变化的本质区别为“是否有新物质生成”,属于基础题.


 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:选择题
| A. | ⅠA族的元素全部都是金属元素 | |
| B. | 元素周期表与18个纵行,即有18个族 | |
| C. | 同周期中的IA族元素的金属性比ⅡA族元素的金属性强 | |
| D. | 元素周期表中右上方区域的元素多用于制造半导体材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2S的水解:S2-+2H2O?H2S+2OH- | |
| B. | NaHCO3的电离:NaHCO3 ?Na++H++CO32- | |
| C. | HSO3-的电离:HSO3-?H++SO32- | |
| D. | 钢铁的电化学腐蚀的负极反应式:Fe-3e-═Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
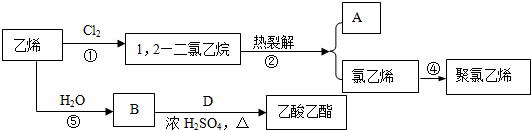
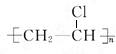 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
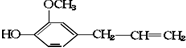 其可能具有的性质是:①能发生加成反应,②能使酸性高锰酸钾溶液褪色,③能发生取代反应,④能与三氯化铁发生显色反应,⑤能发生中和反应,⑥能发生消去反应( )
其可能具有的性质是:①能发生加成反应,②能使酸性高锰酸钾溶液褪色,③能发生取代反应,④能与三氯化铁发生显色反应,⑤能发生中和反应,⑥能发生消去反应( )| A. | 全部 | B. | 仅①②③④ | C. | 除⑥外都能 | D. | 除④⑥外都能 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com