
| 时间/s | 0 | 500 | 1000 | 1500 |
| C(N2O5)/mol/L | 0.50 | 0.35 | 0.25 | 0.25 |
| A. | 500 s时O2的浓度为0.075 mol/L | |
| B. | 平衡后,升高温度,正反应速率先增大后减小 | |
| C. | 平衡后,要使平衡常数增大,改变的条件是升高温度 | |
| D. | 1000 s时将容器的体积缩小一半,重新达到平衡时0.25 mol/L<c(N2O5)<0.50 mol/L |
分析 A.计算N2O5的浓度变化量,浓度变化量之比等于化学计量数之比,据此计算氧气浓度;
B.升高温度反应速率加快,而后N2O5的浓度减小,反应速率又降低;
C.要使平衡常数增大,应改变温度使平衡正向移动,正反应为吸热反应,应升高温度;
D.1000s时反应到达平衡,平衡时c(N2O5)=0.25mol/L,其他条件不变,将容器的体积缩小一半,若平衡不移动,此时N2O5的浓度为0.5mol/L,由于体积减小,压强增大,平衡向逆反应方向移动.
解答 解:A.500s内N2O5的浓度变化量=0.5mol/L-0.35mol/L=0.15mol/L,浓度变化量之比等于化学计量数之比,故c(O2)=$\frac{1}{2}$△c(N2O5)=0.075 mol/L,故A正确;
B.升高温度反应速率加快,而后N2O5的浓度减小,反应速率又降低,故B正确;
C.要使平衡常数增大,应改变温度使平衡正向移动,正反应为吸热反应,应升高温度,故C正确;
D.1000s时反应到达平衡,平衡时c(N2O5)=0.25mol/L,其他条件不变,将容器的体积缩小一半,若平衡不移动,此时N2O5的浓度为0.5mol/L,由于体积减小,压强增大,平衡向逆反应方向移动,则达到新平衡时c(N2O5)>0.5 mol•L-1,故D错误,
故选D.
点评 本题考查化学反应速率计算、化学平衡有关计算、化学平衡影响因素等,侧重考查学生分析计算能力,难度中等,注意对基础知识的理解掌握.


科目:高中化学 来源: 题型:多选题
| A. | 氧化铝坩埚可用于熔融NaOH实验 | |
| B. | 氧化铝的熔点很高,是一种较好的耐火材料 | |
| C. | 明矾可用于自来水的消毒 | |
| D. | 氢氧化铝能中和胃酸,适合于胃溃疡患者服用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg-Cu合金 | B. | Mg-Fe合金 | C. | Al-Zn合金 | D. | Fe-Zn合金 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
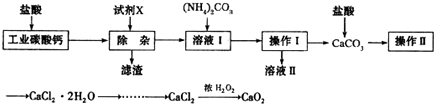
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 0min | 10min | 20min | 30min | 40min | 50min | |
| 830℃ | 1mol | 0.8mol | 0.65mol | 0.55mol | 0.5mol | 0.5mol |
| 1100℃ | 1mol | 0.75mol | 0.6mol | 0.6mol | 0.6mol | 0.6mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 14 | B. | 13 | C. | 12 | D. | 无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
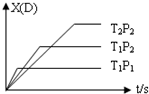 已知可逆反应 mA(g)+nB(g)?pC(g)+qD(g),反应中D的物质的量分数X(D)与时间t的关系如图,则下列叙述正确的是( )
已知可逆反应 mA(g)+nB(g)?pC(g)+qD(g),反应中D的物质的量分数X(D)与时间t的关系如图,则下列叙述正确的是( )| A. | 正反应为放热反应 | B. | m+n>p+q | ||
| C. | T1<T2 | D. | P1<P2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ②④⑤ | C. | ①⑤⑥ | D. | ②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 组别 | 镁铝合金质量.mg | HCl物质的量/mol | 氢气的体积/mL |
| 甲 | 255 | X | 280 |
| 乙 | 385 | X | 336 |
| 丙 | 459 | X | 336 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com