
| 共价键 | H2分子 | N2分子 | NH3分子 |
| 键能(KJ•mo1-1) | 436 | 945 | 391 |
分析 (1)根据反应物、生成物键能的相对大小判断该反应是发热反应还是吸热反应;
(2)根据化学反应的反应热知识,反应物与生成物的键能差即为热量Q1;
(3)合成氨是可逆反应,反应物不能完全转化为生成物.
解答 解:(1)形成化学键放出能量,破坏化学键吸收能量;N2+3H2 2NH3,Q=反应物的键能-生成物的键能=945KJ+3×436-2×3×391KJ=-93KJ<0,所以该反应是放热反应,
2NH3,Q=反应物的键能-生成物的键能=945KJ+3×436-2×3×391KJ=-93KJ<0,所以该反应是放热反应,
故答案为:放热;
(2)Q=反应物的键能-生成物的键能=945KJ+3×436-2×3×391KJ=-93KJ,即放出93KJ热量
故答案为:93kJ;
(3)Q1的数值是按完全转化计算出来的,而合成氨是可逆反应,开始时加入的1molN2和3 molH2不能完全反应生成2molNH3,因而放出热量小于93 kJ,所以,Q1<Q2,
故答案为:B.
点评 本题考查了键能与反应热的关系,形成化学键放出能量,破坏化学键吸收能量,反应热=形成化学键放出能量-破坏化学键吸收能量,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 4:3 | C. | 3:2 | D. | 3:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
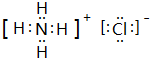 ,化学键类型有离子键、极性键(填“离子键”“极性键”或“非极性键”).
,化学键类型有离子键、极性键(填“离子键”“极性键”或“非极性键”).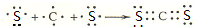 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷的结构式:CH4 | B. | NH4Cl的电子式: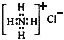 | ||
| C. | 苯的实验式:CH | D. | 乙烯的结构简式:C2H4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过氧化钠电子式: | |
| B. | 质子数35、中子数45的溴原子:${\;}_{35}^{80}$Br | |
| C. | 硫离子结构示意图: | |
| D. | HClO的结构式:H-Cl-O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
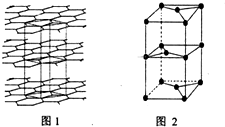
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝热剂 | B. | 黑火药 | C. | 木炭 | D. | 丹药(硫化汞) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com