
������N2H4��������������һ����Ҫ�Ļ��ȼ�ϡ�N2H4��N2O4��Ӧ�ܷų��������ȡ�
��1����֪��2NO2(g)===N2O4(g) ��H=-57.20kJ��mol-1��һ���¶��£����ܱ������з�Ӧ2NO2(g)![]() N2O4(g)�ﵽƽ�⡣������������ʱ�����д�ʩ�����NO2ת���ʵ��� (����ĸ����
N2O4(g)�ﵽƽ�⡣������������ʱ�����д�ʩ�����NO2ת���ʵ��� (����ĸ����
A����СNO2��Ũ��B�������¶� C������NO2��Ũ��D�������¶�
��2��25��ʱ��1.00gN2H4(l)������N2O4(l)��ȫ��Ӧ����N2(g)��H2O(l)���ų�19.14kJ����������Ӧ2N2H4(l)+N2O4(l)=3N2(g)+4H2O(l)�ġ�H= kJ��mol-1��
��3��17�桢1.01��105Pa���ܱ�������N2O4��NO2�Ļ������ﵽƽ��ʱ��c(NO2)=0.0300 mol��L-1��c(N2O4)=0.0120 mol��L-1����Ӧ2NO2(g)![]() N2O4(g)��ƽ�ⳣ��K������������
N2O4(g)��ƽ�ⳣ��K������������

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
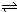 N2O4��g���ﵽƽ�⣮
N2O4��g���ﵽƽ�⣮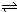 N2O4��g����ƽ�ⳣ��K��
N2O4��g����ƽ�ⳣ��K���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com