
【题目】现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如下图所示(图中有些反应的生成物和反应的条件没有标出)。

请回答下列问题:
(1)写出下列物质的化学式:B_________,丙_________,乙_________,H_________
(2)根据要求回答:
1)D溶液和F溶液在空气中混合的现象:_________________________________;
2)反应③离子方程式___________________________________________________;
3)反应⑦离子方程式___________________________________________________;
4)反应⑥化学方程式___________________________________________________。
【答案】 Al HCl Cl2 Fe(OH)2 产生白色沉淀迅速变成灰绿色,最后变为红褐色 2Al+2OH-+2H2O=2AlO2-+3H2↑ 2Fe2++Cl2=2Cl-+2Fe3+ 4Fe(OH)2+ O2+2H2O=4Fe(OH)3
【解析】金属A焰色反应为黄色,则A为Na,与水反应生成气体甲为H2,D为NaOH,金属B和氢氧化钠溶液反应生成氢气,则B为Al,黄绿色气体乙为Cl2,与氢气反应生成丙为HCl,溶于水得到E为盐酸,物质D(氢氧化钠)和F反应生成H,H在空气中转化为红褐色沉淀I,则H是氢氧化亚铁,I是氢氧化铁,与盐酸反应生成G,则G是氯化铁。F与氯气反应生成G,则F是氯化亚铁,C是铁。
(1)由上述分析可知B、丙、乙、H的化学式分别是;Al、HCl、Cl2、Fe(OH)2;(2)由上述分析可知氢氧化钠溶液和氯化亚铁溶液在空气中混合的现象是产生白色沉淀迅速变成灰绿色,最后变为红褐色;反应③的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑;反应⑦离子方程式为2Fe2++Cl2=2Cl-+2Fe3+;反应⑥化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3。


科目:高中化学 来源: 题型:
【题目】某有机化合物A广泛存在于多种水果中.
(1)经测定,A中仅含有C,H,O三种元素,67gA在空气中完全燃烧时可生成27g H2O和88g CO2 . 则A的实验式或最简式为 . 若要确定A的分子式,还需要知道A的相对分子质量,测定物质的相对分子质量可以采用(填“质谱”或“红外光谱”)法.
经测定A的相对分子质量为134,则A的分子式为 .
(2)又知1molA与足量的NaHCO3溶液充分反应可生成标准状况下的CO2气44.8L,1molA与足量的Na反应可生成1.5mol的H2 , 则A分子中所含官能团的名称为 .
(3)若A分子中不存在甲基且有一个手性碳原子,则A的结构简式为 . 该A在浓硫酸存在下加热,可以生成多种产物,请写出A发生消去反应后所得有机产物的结构简式 .
(4)A的一种同分异构体B,与A所含官能团的种类和数目均相同,且能催化氧化成醛,则B的1H核磁共振谱图中将会出现组特征峰.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 0.012kg12C约含有6.02×1023个碳原子
B. 1mol任何物质都含有6.02×1023个原子
C. 1molFe与足量盐酸反应转移电子数为3NA
D. 常温常压下,1mol氧气的体积为22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向100mL0.01mol/L的HA溶液中逐滴加入0.02mol/L的MOH溶液,图中所示曲线表示混合溶液的pH的变化情况,下列说法正确的是( ) 
A.在N到K间任意一点对应的溶液中:c(M+)+c(H+)=c(OHˉ)+c(Aˉ)
B.HA为弱酸
C.常温下,MA溶液的pH>7
D.N点水的电离程度小于K点水的电离程度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需用2 mol·L-1氯化钠溶液450 mL,配置时应选用容量瓶的规格和称取氯化钠的质量分别是
A. 450 mL,52.7g B.500 mL,58.5g
C.1000 mL,117g D.任意规格,111.2g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将1mol N2O5置于2L密闭容器中,在一定温度下发生下列反应: ①2N2O5(g)2N2O4(g)+O2(g);②N2O4(g)2NO2(g).达到平衡时,c(O2)=0.2molL﹣1 , c(NO2)=0.6molL﹣1 , 则此温度下反应①的平衡常数为( )
A.3.2
B.0.2
C.![]()
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2和NOx是主要的大气污染物。某小组认为一定条件下,用NH3与NO2反应转化为无污染物质可进行汽车尾气无害化处理。
(1)氨气的制备
①实验室制氨气的化学方程式为_________。
②制备和收集纯净、干燥的氨气,可以选择下图装置______(填序号),C中试剂为______。

(2)氨气与二氧化氮的反应(已知:2NO2+2NaOH=NaNO3+NaNO2+H2O。)
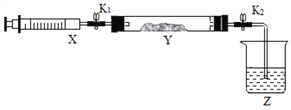
①在硬质玻璃管Y中加入少量催化剂,将NO2气体注入Y管中,Z中应盛装______。
②打开K1,将注射器X中的NH3缓慢注入Y中,发生反应的方程式为_______。
③将注射器活塞退回原处并固定,待装置恢复到室温,打开K2,Y中出现倒吸现象,原因是_________。
(3)该小组进一步研究SO2的性质,探究SO2能否与Na2O2发生氧化还原反应。实验室用铜丝和浓硫酸反应生成SO2的化学方程式为____________。利用(2)中装置,将Y中的药品更换为少量Na2O2,将注射器X中SO2缓慢推入Y中,Y装置中淡黄色粉末变成白色。设计方案检验生成的白色物质中含有SO42-_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com