
| A. | CH3CH2CH2CH3(3个) | B. | 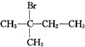 (2个) (2个) | ||
| C. | CH2=CH-CH2CH3(3个) | D. | 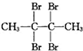 (1个) (1个) |
科目:高中化学 来源: 题型:选择题
| A. | a-n | B. | a+m | C. | a-m | D. | a+n |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
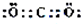 .过量该物质与偏铝酸钠溶液反应的离子方程式为AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-.
.过量该物质与偏铝酸钠溶液反应的离子方程式为AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A原子的最外层电子数比B原子的最外层电子数少 | |
| B. | 常温时,A能从盐酸中置换出氢气,而B不能反应 | |
| C. | B不能从溶液中置换出A | |
| D. | 1 mol A失去的电子比1 mol B失去的电子多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:A>B>C>D | B. | 离子半径:C>D>B>A | ||
| C. | 原子序数:d>c>b>a | D. | 最外层电子数:D>C>B>A |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在金属区、非金属区交界线上,寻找具有半导体性能的材料 | |
| B. | 形成化合物种类最多的元素在第14列 | |
| C. | 第ⅡA族的右边是第ⅢB族,第ⅢA族的左边是第ⅡB族 | |
| D. | 某主族元素最高价氧化物对应的水化物的化学式为HnROm,其气态氢化物的化学式一定为H2m-nR或RH2m-n |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4 C2H2 | B. | C2H6 C3H6 | C. | C2H4 C3H6 | D. | C2H4 C3H4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钠溶液中通入少量二氧化硫气体 SO2+OH-═HSO3- | |
| B. | 向硫酸铝中加入过量氨水:Al3++4NH3•H2O═AlO2-+2H2O+4NH4+ | |
| C. | NH4HCO3溶液与足量NaOH溶液共热:NH4++HCO3-+2OH-$\frac{\underline{\;\;△\;\;}}{\;}$ NH3↑+2H2O+CO32- | |
| D. | 浓硝酸中加入过量铁粉并加热:Fe+3NO3-+6H+$\frac{\underline{\;\;△\;\;}}{\;}$ Fe3++3NO2↑+3H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com