
| A. | 加成→消去 | B. | 加成→水解 | C. | 消去→加成 | D. | 消去→取代 |
科目:高中化学 来源: 题型:选择题
| A. | 原子的核外电子排布呈周期性变化 | B. | 原子半径呈周期性变化 | ||
| C. | 原子的电子层数呈周期性变化 | D. | 化合价呈周期性变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢键 分子间作用力 非极性键 | |
| B. | 氢键 极性键 分子间作用力 | |
| C. | 氢键 氢键 极性键 | |
| D. | 分子间作用力 氢键 非极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 与等体积、pH=3的盐酸比较,跟足量锌粒反应产生的H2更少 | |
| B. | 加水稀释到原体积的10倍后溶液pH变为4 | |
| C. | 加入少量乙酸钠固体,溶液pH升高 | |
| D. | 升高温度,溶液中所有离子浓度均增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
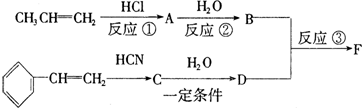
 .
.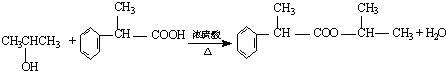 .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| 元素编号 | 元素性质或原子结构 |
| X | M层的电子数是原子核外电子层数的2倍 |
| Y | 最高价氧化物既能与强酸反应,又能与强碱反应 |
| Z | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| T | 最高价氧化物的水化物为无机酸中最强的酸 |
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 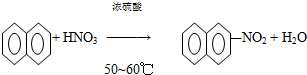 | |
| B. | CH3CH2CH2CHOHCH3$→_{△}^{浓硫酸}$CH3CH2CH=CHCH3+H2O | |
| C. | CH3CHO+H2$→_{催化剂}^{高温高压}$CH3CH2OH | |
| D. | 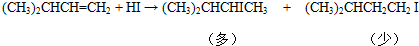 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙酸乙酯中含乙酸杂质:加入饱和碳酸钠溶液洗涤,分液 | |
| B. | 乙醇中含乙酸杂质:加入碳酸钠溶液洗涤,分液 | |
| C. | 乙醛中含乙酸杂质:加入氢氧化钠溶液洗涤,分液 | |
| D. | 苯中含苯酚杂质:加入浓溴水,过滤 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com