
����ij�¶���ƽ����ϵmA(g) + nB(g) pC(g) + qD(g) ��H<0������˵������ȷ����
pC(g) + qD(g) ��H<0������˵������ȷ����
A�����¶Ȳ��佫�����ݻ�����ԭ����2������ʱA��Ũ�ȱ�Ϊԭ����0.52������m + n > p + q
B����ƽ����ϵ�м���C��D���÷�Ӧ�ġ�H��С
C�����¶Ⱥ�����������䣬����һ�����Ķ������壬B��Ũ�Ȳ���
D����ƽ��ʱ������A������A��ת�����½���B��ת��������
B
��������
���������A�����¶Ȳ��佫�����ݻ�����ԭ����2������ƽ�ⲻ�ƶ�����A��Ũ�ȱ�Ϊԭ����0.5������ʱA��Ũ�ȱ�Ϊԭ����0.52����˵���������ѹǿ��С��ƽ�������ƶ������������������ʵ�������ķ�������m+n>p+q����ȷ��B����Ӧ�������ʵ�״̬������ʽ�з�Ӧ���ϵ���йأ���ʵ�ʷ�Ӧ�����ʵ����أ����Ը÷�Ӧ�ġ�H���䣬����C�����¶Ⱥ�����������䣬����һ�����Ķ������壬����Ӧ��ϵ�и����ʵ�Ũ�Ⱦ����䣬����ƽ�ⲻ�ƶ���B��Ũ�Ȳ��䣬��ȷ��D�����ڶ��ַ�Ӧ��ķ�Ӧ������һ�����ʵ������������������ʵ�ת���ʣ���������ת���ʽ��ͣ�����ƽ��ʱ������A������A��ת�����½���B��ת�������ӣ���ȷ����ѡB��
���㣺����������ƽ���ƶ���Ӱ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014��㶫ʡ�����и߶���ѧ�����п��Ի�ѧ���ģ��Ծ��������棩 ���ͣ�ѡ����
��ij���˵���Һ�������Ƶ�Cu(OH)2��Һ�У���ʱ����۲쵽��ɫ������˵������Һ�к���
A������ B�������� C��ʳ�� D���ƾ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�ﰲ��ʡ��һ��ѧ�����л�ѧ�Ծ��������棩 ���ͣ������
(8��)����ʱ������ͬѧ�Ʊ�Fe(OH)3���壬����������£�
�������ձ��м���25 mL����ˮ���þƾ��Ƽ��������ڣ�Ȼ�����ձ�����εμ�6��FeCl3������Һ�������������Һ������ĺ��ɫ������Fe(OH)3���塣
�Իش��������⣺
��1��д���÷�Ӧ�Ļ�ѧ����ʽ________________________________________
��2�����֤������ͬѧ�Ƿ�ɹ��Ƶý��壿_________________________________________
��3��������ͬѧ�ڵμ�FeCl3������Һ��ͬʱ�ò��������Ͻ��裬���û�еõ����壬Ϊʲô�أ�_________________________________________________________________
��4������ͬѧ�Ƶõ�Fe(OH)3�����к����������ᣬΪ�õ��ϴ����Ľ��壬������������²�������������____ ____��
A������NaOH��Һ�����к�
B������AgNO3��Һ��Ӧ�����
C��װ���Ĥ���У��������ڣ�����ȫ����������ˮ�У���ÿ��һ��ʱ�䣬����һ������ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�ﰲ��ʡ��һ��ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й��Ƶ������У��������
A���ƵĻ�ԭ�Ժ�ǿ����������ұ�������ѡ�ﯡ����
B���ƵĻ�ѧ���ʷdz����ã���Ԫ��ֻ���Ի���̬��������Ȼ��
C������һ�ֻҺ�ɫ�Ĺ���
D���Ƶ��ʵؽ���������С���и�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�ﰲ��ʡ�����и߶���ѧ�����л�ѧ�������Ծ��������棩 ���ͣ�ѡ����
���淴Ӧ��2NO2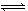 2NO+O2�ں��º����ܱ������з�Ӧ���ﵽƽ��״̬�ı�־��
2NO+O2�ں��º����ܱ������з�Ӧ���ﵽƽ��״̬�ı�־��
�ٵ�λʱ��������n molO2��ͬʱ����2n molNO2
�ڵ�λʱ��������n molO2 ��ͬʱ����2n mol NO
����NO2��NO��O2 �����ʵ���Ũ�ȱ仯��ʾ�ķ�Ӧ���ʵı�Ϊ2 : 2 : 1��״̬
�ܻ���������ɫ���ٸı��״̬
�ݻ��������ܶȲ��ٸı��״̬
��������ƽ����Է����������ٸı��״̬
A���٢ܢ� B���ڢۢ� C���٢ۢ� D���٢ڢۢܢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�ﰲ��ʡ�����и߶���ѧ�����л�ѧ�������Ծ��������棩 ���ͣ�ѡ����
��N2 (g)�� 3H2(g) 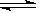 2 NH3 (g)��ƽ����ϵ��,������������,���ӵ�����Ũ��,�����ж���ȷ����
2 NH3 (g)��ƽ����ϵ��,������������,���ӵ�����Ũ��,�����ж���ȷ����
A.������ת��������
B.������ת��������
C.������ƽ���������еİٷֺ���һ������
D.�����ķֽ����ʴ��ڰ�������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�ﰲ��ʡ�����и߶���ѧ�����л�ѧ�������Ծ��������棩 ���ͣ�ѡ����
����ʵ���У���Ӧ���ʼӿ����ɴ����������
A����̿���м���KClO3 ����ȼʱȼ�ո�Ϊ����
B��H2O2�м�������FeCl3������Ѹ�ٷų�����
C����̿�����ɷ�ĩ״����ʹȼ�ո��ӳ��
D��п��ϡ���ᷴӦ�м�����������ͭ�������������ʼӿ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�ﰲ��ʡ�����и�һ��һѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵���У���ȷ����
A��ʧȥ���ӵ������ǻ�ԭ��������������
B��������ԭ��Ӧ�ı�����Ԫ�ػ��ϼ۵�����
C��������ԭ��Ӧ�У�ijԪ���ɻ���̬��Ϊ����̬,��Ԫ�ؿ��ܱ���ԭ������
D����������ԭ��Ӧ�У����Ӳ�������ͬ��Ԫ�ؼ�ת��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�^����ʡ�����и߶���һѧ���������ƻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��10�֣����³�ѹ�£�����1mol������ӻ�ѧ�������յ��������γ�1mol������ӻ�ѧ�����ų���������Ϊ���ܣ���λΪkJ.mol-1���������±��������ݣ�kJ��mol��1���ش����⣺
��ѧ�� | C��F | C��Cl | C��I | H��H | S��S | H��S |
���� | 427 | 330 | 218 | 436 | 255 | 339 |
��1���ɱ�������Ԥ��C��Br���ļ��ܷ�Χ��_________��C��Br���ܣ�_________���ش���ֵ�͵�λ��
��2���Ȼ�ѧ����ʽ2H2(g)��S2(g) = 2H2S(g)����H= QkJ��mol��1����Q=
��3����֪�����Ȼ�ѧ����ʽ��
��O2 (g) = O+2(g) + e- 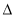 H1= +1175.7 kJ��mol-1 ��PtF6(g) + e- = PtF6��(g)
H1= +1175.7 kJ��mol-1 ��PtF6(g) + e- = PtF6��(g) 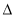 H2= -771.1 kJ��mol-1
H2= -771.1 kJ��mol-1
��O2+PtF6-(s) = O2+(g) + PtF6-(g)  H3= +482.2 kJ��mol-1
H3= +482.2 kJ��mol-1
��ӦO2(g) + (g) = O2+PtF6-(s) 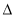 H=_____________ kJ��mol-1��
H=_____________ kJ��mol-1��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com