
����Ŀ��������ϩ��PVC������Ĥ�İ�ȫ��������㷺��ע��PVC�İ�ȫ������Ҫ�����������в�����PVC�����Լ������Ϲ��ұ������ܼ�DEHA����ҵ������ϩ������Ϊԭ�Ͼ����и����ϳ�PVC��
![]()
��1������PVC�ĵ��壬��ṹ��ʽΪ_____________________��
��2����Ӧ�ٵĻ�ѧ����ʽΪ______________________________________________________��
��3��д�����·�Ӧ���ͣ���Ӧ��_________________����Ӧ��_________________��
��4���ڱ�������������DOP���ǹ��ұ�������ʹ�õ����ܼ�֮һ���ڱ������ᣨ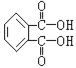 ��������DOP��ԭ�ϣ����������ļ״���Ӧ�ܵõ���һ�����ܼ�DMP������ʽΪC10H10O4����DMP���ڷ���������д��DMP�Ľṹ��ʽΪ________________��
��������DOP��ԭ�ϣ����������ļ״���Ӧ�ܵõ���һ�����ܼ�DMP������ʽΪC10H10O4����DMP���ڷ���������д��DMP�Ľṹ��ʽΪ________________��
���𰸡� CH2=CHCl CH2=CH2 + Cl2![]() CH2ClCH2Cl ��ȥ��Ӧ �Ӿ۷�Ӧ
CH2ClCH2Cl ��ȥ��Ӧ �Ӿ۷�Ӧ 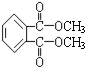
����������1��CH2=CH2�������������ӳɷ�Ӧ����CH2ClCH2Cl��CH2ClCH2Cl������ȥ��Ӧ����CH2=CHCl��CH2=CHCl�����Ӿ۷�Ӧ������PVC�����ΪCH2ClCH2Cl����ΪCH2=CHCl���ʴ�Ϊ��CH2=CHCl�� ��2����Ӧ��ΪCH2=CH2 + Cl2![]() CH2ClCH2Cl����Ӧ��CH2ClCH2Cl
CH2ClCH2Cl����Ӧ��CH2ClCH2Cl![]() CH2=CHCl+HCl��������ȥ��Ӧ����Ӧ��������ϩ�����Ӿ۷�Ӧ���ɾ�����ϩ����Ӧ����Ϊ�Ӿ۷�Ӧ����3���Ա��ڱ�������Ľṹ��DMP�ķ���ʽ��֪��ӦΪ�ڱ��������2���ļ״�����������Ӧ����DMP����DMP�Ľṹ��ʽΪ��
CH2=CHCl+HCl��������ȥ��Ӧ����Ӧ��������ϩ�����Ӿ۷�Ӧ���ɾ�����ϩ����Ӧ����Ϊ�Ӿ۷�Ӧ����3���Ա��ڱ�������Ľṹ��DMP�ķ���ʽ��֪��ӦΪ�ڱ��������2���ļ״�����������Ӧ����DMP����DMP�Ľṹ��ʽΪ��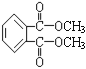 ��
��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й����ʵķ�����ȷ���ǣ�������
A. SO2��SiO2��CO������������
B. ϡ���������ᡢ�Ȼ�����Һ��Ϊ����
C. ���ᡢ���ᡢ������Ϊǿ��
D. ��ˮ��ˮ��������ˮ��Ϊ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����K2Cr2O7��14HCl===2KCl��2CrCl3��3Cl2����7H2O��Ӧ�С�
(1) ________Ԫ�ر�������________����������
(2)________���������________����������Ӧ��
(3)��˫���ŷ���������ת�Ƶķ������Ŀ___________________________________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧС����ͼʾװ����ȡ����������˵������ȷ����(����)
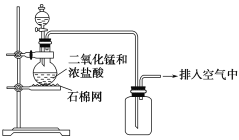
A. ��װ��ͼ�����ٴ����������Դ���
B. Ϊ�˷�ֹ������Ⱦ�������������β������
C. �ڼ���ƿ�ĵ��ܿڴ���һƬʪ��ĵ��۵⻯����ֽ����֤���Ƿ��������ݳ�
D. ��ʵ�����ռ������ķ�������ȷ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ģ������ģ�8�ǻ�������㷺�����������ӵ���ϼ�����ȡ����Ҳ����Ҫ��ҽҩ�м��塣��ͼ��8�ǻ�����ĺϳ�·�ߡ�
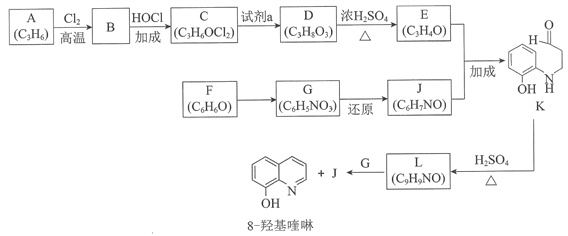
��֪��i. 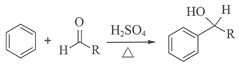
ii.ͬһ��̼ԭ��������2���ǻ��ķ��Ӳ��ȶ���
��1���������ŷ��࣬A�������__________��
��2��A��B�Ļ�ѧ����ʽ��____________________��
��3��C���ܵĽṹ��ʽ��__________��
��4��C��D������Լ�a��__________��
��5��D��E�Ļ�ѧ����ʽ��__________��
��6��F��G�ķ�Ӧ������__________��
��7��������K��L������ͼ����������____________

��8���ϳ�8�ǻ����ʱ��L������__________�����������ԭ������Ӧ����Ӧʱ��������ˮ����L��G���ʵ���֮��Ϊ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ��С���Ʊ�������أ�K2FeO4����̽�������ʡ�
���ϣ�K2FeO4Ϊ��ɫ���壬����KOH��Һ������ǿ�����ԣ������Ի�������Һ�п��ٲ���O2���ڼ�����Һ�н��ȶ���
��1���Ʊ�K2FeO4���г�װ���ԣ�
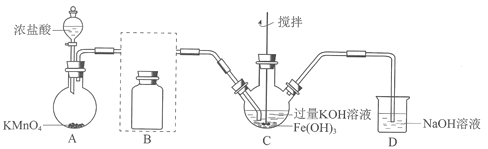
��AΪ��������װ�á�A�з�Ӧ����ʽ��________________���̱���ԭΪMn2+����
�ڽ�����װ��B�������������������Լ���_______
��C�еõ���ɫ�������Һ��C��Cl2�����ķ�Ӧ��
3Cl2+2Fe(OH)3+10KOH![]() 2K2FeO4+6KCl+8H2O�������________________��
2K2FeO4+6KCl+8H2O�������________________��
��2��̽��K2FeO4������
��ȡC����ɫ��Һ������ϡ���ᣬ��������ɫ���壬����Һa�������������к���Cl2��Ϊ֤���Ƿ�K2FeO4������Cl��������Cl2��������·�����
������ | ȡ����a���μ�KSCN��Һ����������Һ�ʺ�ɫ�� |
������ | ��KOH��Һ���ϴ��C�����ù��壬����KOH��Һ��K2FeO4�ܳ����õ���ɫ��Һb��ȡ����b���μ����ᣬ��Cl2������ |
i���ɷ���������Һ����֪a�к���______���ӣ��������ӵIJ��������ж�һ����K2FeO4��Cl����������������________________�������÷���ʽ��ʾ����
ii���������֤��K2FeO4������Cl������KOH��Һϴ�ӵ�Ŀ����________________��
�ڸ���K2FeO4���Ʊ�ʵ��ó���������Cl2________![]() �����������������������ʵ�������Cl2��
�����������������������ʵ�������Cl2��![]() ��������ǿ����ϵ�෴��ԭ����________________��
��������ǿ����ϵ�෴��ԭ����________________��
�����ϱ�����������Һ�е�������![]() ��
��![]() ����֤ʵ�����£�����Һb����MnSO4������H2SO4�Ļ����Һ�У�����Һ��dz��ɫ���������ܷ�֤��������
����֤ʵ�����£�����Һb����MnSO4������H2SO4�Ļ����Һ�У�����Һ��dz��ɫ���������ܷ�֤��������![]() ��
��![]() �����ܣ���˵�����ɣ������ܣ���һ�����ʵ�鷽����
�����ܣ���˵�����ɣ������ܣ���һ�����ʵ�鷽����
���ɻ���________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
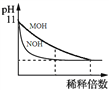
����Ŀ������ͼʾ���Ӧ�������������
�� �� �� ��
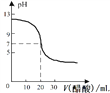
A. ͼ�ױ�ʾ������ϡ��pH��Ϊ11��MOH��Һ��NOH��ҺʱpH�ı仯����ͼ��֪��Һ�ļ��ԣ�MOH��NOH
B. ͼ�ұ�ʾ������0.100 0 mol��L��1������Һ�ζ�20.00 mL0.100 0 mol��L��1 NaOH��Һ�ĵζ�����
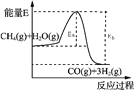
C. ͼ����ʾ��ӦCH4(g)��H2O (g)![]() CO(g)��3H 2(g)�������仯��ʹ�ô����ɸı�Eb��Ea��ֵ
CO(g)��3H 2(g)�������仯��ʹ�ô����ɸı�Eb��Ea��ֵ
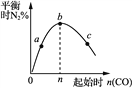
D. ͼ����ʾ��Ӧ2CO(g)��2NO(g)![]() N2(g)��2CO2(g)����������������ʱ���ı���ʼCO�����ʵ�����ƽ��ʱN2����������仯����ͼ��֪NO��ת����c��b��a
N2(g)��2CO2(g)����������������ʱ���ı���ʼCO�����ʵ�����ƽ��ʱN2����������仯����ͼ��֪NO��ת����c��b��a
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ԫ�������ˮ�帻Ӫ��������Ҫԭ����ˮ�г�������NO3��ʽ���ڡ�
��1����pHΪ4��6ʱ����H2��Pd-Cu���½�NO3-��ԭΪN2������ˮ��NO3���÷�Ӧ�����ӷ���ʽΪ____������H2��CO2�Ļ���������H2��NO3-ȥ��Ч�����ã���ԭ����____��
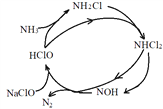
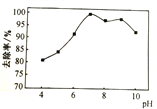
��2��NaClO�����ɳ�ȥ��������Ӧ������ͼ1��ʾ������H2O��NaCl��ȥ����ʵ������ͬ�����£���ͬ��Ӧʱ�䣬pH�백����ȥ���ʹ�ϵ��ͼ2��ʾ���¶��백��ȥ���ʹ�ϵ��ͼ3��ʾ��

ͼ1 ͼ2 ͼ3
��NaClO����NH3���ܷ�Ӧ�Ļ�ѧ����ʽΪ____��
����ͼ2��ʾ����pH��9ʱ��pHԽ��ȥ����ԽС����ԭ����____��
����ͼ3��ʾ���¶ȵ���15��ʱ���¶�Խ��ȥ����Խ����ԭ����____�����¶ȸ���25��ʱ���¶�Խ��ȥ����ҲԽ�ͣ���ԭ����____��
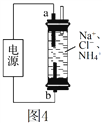
��3���õ绯ѧ����ȥ����ˮ�еİ������ں�NH4+�ķ�ˮ�м����Ȼ��ƣ��ö��Ե缫��⡣��Ӧװ����ͼ4��ʾ������ʱ��a���ĵ缫��ӦʽΪ____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NaOH��MgCl2��AlCl3���ֹ�����ɵĻ������������ˮ�к���1.16g��ɫ����,�����õ�����Һ����μ���1mol��L-1HCl��Һ,����HCl��Һ�����V�����ɳ���������m�Ĺ�ϵ��ͼ��ʾ���Իش�

(1)A�������Ļ�ѧʽΪ_____________��
(2)AlCl3�����ʵ���Ϊ________________��
(3)HCl��Һ��Q��ļ�������_________________
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com