
 甲醇是一种重要的化工原料.
甲醇是一种重要的化工原料.| CO2%-CO%-H2% (体积分数) | 0-30-70 | 2-28-70 | 4-26-70 | 8-22-70 | ||||||||
| 反应温度/℃ | 225 | 235 | 250 | 225 | 235 | 250 | 225 | 235 | 250 | 225 | 235 | 250 |
| 生成CH3OH的碳转化率(%) | 4.9 | 8.8 | 11.0 | 36.5 | 50.7 | 68.3 | 19.0 | 33.1 | 56.5 | 17.7 | 33.4 | 54.4 |
分析 (1)利用盖斯定律,①-②×4即可得到目标方程式,据此计算反应热即可;
(2)①依据平衡常数为生成物的浓度幂之积比反应物的浓度幂之积;
②为使甲醇与二氧化碳的物质的量比值增大,应使平衡向正反应方向移动,或增加甲醇的物质的量;
(3)NaOH和甲酸恰好反应时生成强碱弱酸盐,溶液呈碱性,若要呈中性,则甲酸过量;
(4)甲醇碱性燃料电池中,负极上甲醇失电子和氢氧根离子反应生成碳酸根离子和水,正极上氧气得电子和水反应生成氢氧根离子,据此书写电极反应式;
(5)由表格分析得出结论:在一定条件下,反应温度越高,生成甲醇的碳转化率越高;原料气含少量CO2有利于提高生成甲醇的碳转化率,CO2含量过高生成甲醇的碳转化率又降低.
解答 解:(1)根据盖斯定律,将①-②×4可得:2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=(-1275.6kJ/mol)-(+44.0kJ/mol)×4=-1451.6kJ/mol,所以表示甲醇燃烧热的热化学方程式为:CH3OH(l)+3/2 O2(g)=CO2(g)+2H2O(l)△H=-725.8kJ/mol,
故答案为:CH3OH(l)+3/2 O2(g)=CO2(g)+2H2O(l)△H=-725.8kJ/mol;
(2)①CH3OH (g)+H2O (g)?CO2(g)+3H2(g)△H=-72.0kJ/mol,该反应的平衡常数表达式为K=$\frac{c(C{O}_{2}){c}^{3}({H}_{2})}{c(C{H}_{3}OH)c({H}_{2}O)}$,故答案为:K=$\frac{c(C{O}_{2}){c}^{3}({H}_{2})}{c(C{H}_{3}OH)c({H}_{2}O)}$;
②CH3OH (g)+H2O (g)?CO2(g)+3H2(g),反应是气体体积增大的反应;
A、加入催化剂,平衡向不发生移动,甲醇与二氧化碳的物质的量比值不变,故A错误;
B、恒容充入He(g),使体系压强增大,分压不变,对反应物质没有影响,平衡不移动,二者比值不变,故B错误;
C、将H2(g)从体系中分离,生成物的浓度减小,平衡向正反应方向移动,二者比值变大,故C正确;
D、再充入1mol H2O,平衡向正方向移动,甲醇浓度增大,二者比值增大,故D正确.
故答案为:CD;
(3)NaOH和甲酸恰好反应时生成强碱弱酸盐,溶液呈碱性,若要呈中性,则甲酸过,所以滴定到pH=7时,V(NaOH)<20.00ml,故答案为:<;
(4)甲醇碱性燃料电池中,负极上甲醇失电子和氢氧根离子反应生成碳酸根离子和水,电极反应式为2CH3OH-12e-+16OH-=2CO32-+12H2O,故答案为:2CH3OH-12e-+16OH-=2CO32-+12H2O;3O2+12H2O+12e-=12OH-;
(5)由表格中原料气各组分含量不同时反应生成甲醇的碳转化率的数据可知:反应温度越高,生成甲醇的碳转化率越高;二氧化碳的体积分数为2%时生成甲醇的碳转化率最高,二氧化碳的体积分数为20%生成甲醇的碳转化率较低,不含二氧化碳时生成甲醇的碳转化率最低,因此原料气含少量CO2有利于提高生成甲醇的碳转化率,CO2含量过高生成甲烷的碳转化率又降低,故答案为:越高;原料气含少量CO2有利于提高生成甲醇的碳转化率,CO2含量过高生成甲烷的碳转化率又降低越高.
点评 本题考查学生有关化学平衡的有关知识,主要是表格中数据的收集、分析、处理能力要求颇高,难度较大.


科目:高中化学 来源: 题型:选择题
| A. | 生物酶固氮相比人工固氮更高效、条件更温和 | |
| B. | 近日用地沟油炼制的生物航油载客首飞,标志着我国航空业在节能减排领域进入商业飞行阶段 | |
| C. | 分光光度计不能用于测定草酸与高锰酸钾的反应速率 | |
| D. | 尿液燃料电池的原理是在微生物作用下将尿液中的有机物转化为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 规律(或性质) | 结 论 |
| A | 主族元素最高正化合价等于族序数 | 第VⅡA族元素最高正价都是+7 |
| B | SO2和湿润的Cl2都有漂白性 | 二者混合后漂白性更强 |
| C | 常湿下铜与浓硝酸反应可以制取NO2 | 常温下铁与浓硝酸反应也可以制取NO2 |
| D | 较强酸可以制取较弱酸 | CO2通入NaClO溶液液中能生成HC10 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
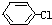 +NaOH→
+NaOH→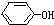 +NaCl,该反应的反应类型属于( )
+NaCl,该反应的反应类型属于( )| A. | 加成反应 | B. | 取代反应 | C. | 氧化还原反应 | D. | 置换反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
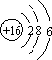 ;羰基硫分子的电子式为
;羰基硫分子的电子式为 .
.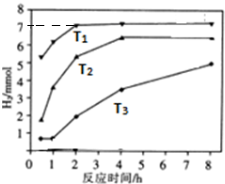
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
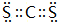 ,Y3-的立体构型为直线形.
,Y3-的立体构型为直线形.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
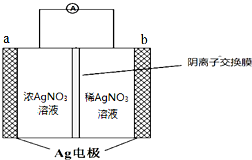 银是一种在工业、生活上有广泛用途的金属.
银是一种在工业、生活上有广泛用途的金属.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (3m+n)mol | B. | (3m+n+2p)mol | C. | (2.5m+0.5n-3p)mol | D. | (2.5m+0.5n)mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com